
| 19.2g |
| 64g/mol |
| 1 |
| 4 |
| 19.2g |
| 64g/mol |
| 1 |
| 4 |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
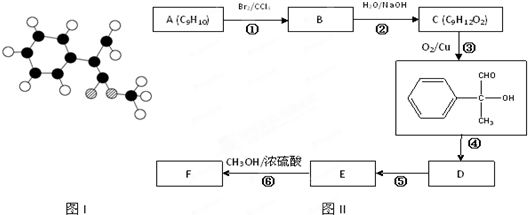
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、该反应中氧化剂是氧气 |
| B、铜是导电性最好的金属 |
| C、可以将铜的冶炼和硫酸的生产联合在一起 |
| D、在Cu2S中铜的化合价为+2价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
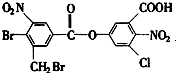 与足量的NaOH溶液混合,在一定条件下反应,则NaOH的物质的量共消耗了( )
与足量的NaOH溶液混合,在一定条件下反应,则NaOH的物质的量共消耗了( )| A、8 mol |
| B、6 mol |
| C、5 mol |
| D、4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一氯胺中氯元素的化合价为-1价 |
| B、一氯胺水解的产物为NH2OH(羟氨)和HCl |
| C、一氯胺起消毒作用的物质与漂白粉起消毒作用的物质相同 |
| D、一氯胺的摩尔质量为51.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用滤纸称量氢氧化钠固体 |
| B、溶解后未冷却直接定容 |
| C、容量瓶不干燥,存有少量蒸馏水 |
| D、胶头滴管加水定容时仰视刻度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在NaHA溶液中c(Na+)>c (HA-)>c(H+)>c (OH-) |
| B、在Na2A溶液中c (Na+)=2c (A2-)+2c(HA-)+2c (H2A) |
| C、在Na2A溶液中 c (OH-)=c (HA-)+c (H+) |
| D、在H2A溶液中c (H+)=c (HA-)+2c (A2-)+c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤化氢分子中,卤素的非金属性越强,共价键的极性也越大,稳定性也越强 |
| B、H2O中O-H键之间的键角大于H2S中S-H键之间的键角 |
| C、具有极性键且空间构型不对称的A2B或AB2型分子为极性分子 |
| D、非极性分子中只存在非极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com