
分析 pH=a的强酸稀释10b倍时,溶液的pH=a+b(a+b<7,若a+b>7,则让a+b=7);
pH=a的弱酸稀释10b倍时,溶液的pH<a+b(a+b<7);
将酸溶液稀释时,氢离子浓度降到10-7mol/L即不再下降,但硫酸根会一直降低;
pH=c的强酸稀释10d倍时,溶液的pH=c-d(c-d>7,若c-d<7,则让c-d=7);
对盐溶液加水稀释,盐的水解被促进,据此分析溶液的pH变化.
解答 解:由于pH=a的强酸稀释10b倍时,溶液的pH=a+b(a+b<7,若a+b>7,则让a+b=7),故pH=3的HCl稀释100倍后溶液的pH变为3+2=5;
pH=a的弱酸稀释10b倍时,溶液的pH<a+b(a+b<7),由于醋酸是弱酸,故将pH=3的HAc溶液稀释100倍后pH<3+2=5,故若时pH变为5,则稀释的倍数应大于100;
将酸溶液稀释时,氢离子浓度降到10-7mol/L即不再下降,但硫酸根会一直降低,即pH=5的稀硫酸溶液中[H+]=10-5mol/L,而[SO42-]=$\frac{1}{2}$×10-5mol/L,稀释1000倍后溶液中[H+]=10-7mol/L,而[SO42-]=$\frac{\frac{1}{2}×1{0}^{-5}mol/L}{1000}$=5×10-9mol/L,即溶液中[H+]:[SO42-]=20:1;
pH=c的强酸稀释10d倍时,溶液的pH=c-d(c-d>7,若c-d<7,则让c-d=7),故pH=10的Na0H溶液稀释100倍后溶液的pH变为10-2=8;
对盐溶液加水稀释,盐的水解被促进,故溶液的pH大于9.
故答案为:5;小于5;>;20:1;8;大于9.
点评 本题考查了酸和碱稀释后溶液的pH的变化规律,难度不大,应注意的是酸溶液稀释后,溶液中的氢离子浓度降到10-7mol/L即不再下降,但硫酸根会一直降低.


科目:高中化学 来源: 题型:解答题
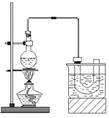 实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:
实验室制备溴乙烷(C2H5Br)的装置和步骤如下:(已知溴乙烷的沸点38.4℃)①检查装置的气密性,向装置图所示的∪形管和大烧杯中加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL78%浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小心加热,使其充分反应.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
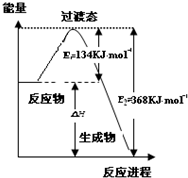 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 与铝反应产生氢气的溶液中:Na+、NH4+、SO42-、CH3C00- | |
| B. | c(Fe3+)=0.1mol•L-1的溶液中:NH4+、Cl-、AlO2-、SO42- | |
| C. | 使甲基橙变红的溶液中:K+、Al3+、SO42-、NO3- | |
| D. | 由水电离出的c(OH-)=10-13mol•L-1的溶液中:Na+、Ba2+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{b-a}{b}$ | B. | $\frac{2(b-a)}{b}$ | C. | $\frac{3a-2b}{b}$ | D. | $\frac{2b-3a}{b}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
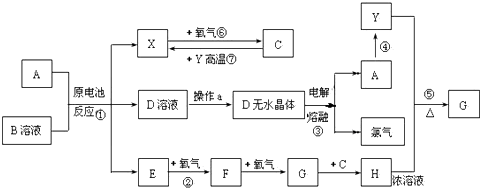
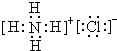
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 相对原子质量 | 密度/(g.cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.813 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊醇 | 130 | 0.8670 | 142 | 难溶 |
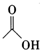 +
+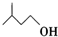 $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ 
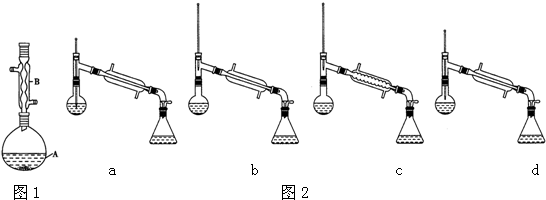
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com