



 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
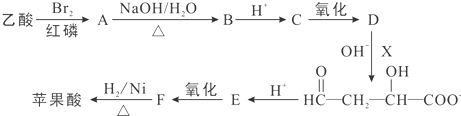
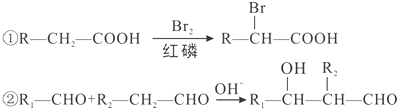
查看答案和解析>>
科目:高中化学 来源: 题型:
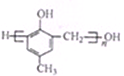 )的合成路线如下:
)的合成路线如下: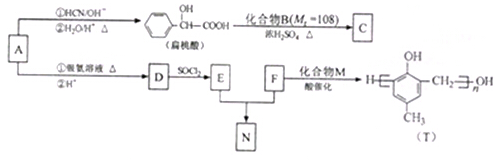
| ||
| ②H2O,H+△ |
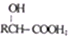
| SOCl2 |

| R′OH |
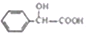 )有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有
)有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有查看答案和解析>>
科目:高中化学 来源: 题型:
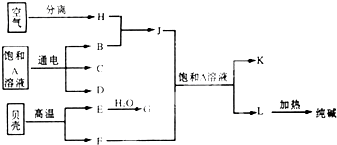 以海水中常见的物质A为原料可以发展很多种工业,如图中包含了几种基本工业生产,请根据各物质之间的转化关系.回答下列问题:
以海水中常见的物质A为原料可以发展很多种工业,如图中包含了几种基本工业生产,请根据各物质之间的转化关系.回答下列问题:| 水 |
| 溶解 |
| 过量BaCl2溶液 |
| 过滤 |
| 水 |
| 洗涤 |
| 低温烘干、冷却、称重 |
查看答案和解析>>
科目:高中化学 来源: 题型:
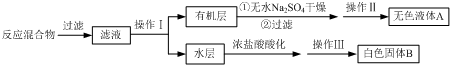

查看答案和解析>>
科目:高中化学 来源: 题型:
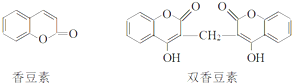
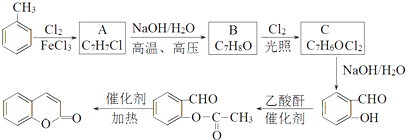
 与乙酸酐(
与乙酸酐( )反应,除生成
)反应,除生成 外,另一种产物是
外,另一种产物是查看答案和解析>>
科目:高中化学 来源: 题型:

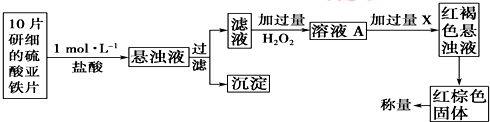
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com