
| A. | 1 | B. | 10 | C. | 104 | D. | 10-4 |
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 49 个 | B. | 50个 | C. | 51个 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
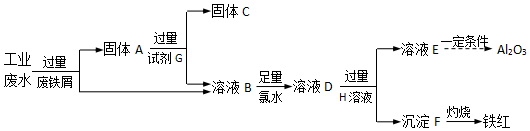
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| Al2O3 | Na2O2 | Si | Na2SiO3 |
| 两性氧化物 | 碱性氧化物 | 单质 | 硅酸盐 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发时,蒸发皿中固体不能蒸干才停止加热 | |
| B. | 蒸馏时,温度计水银球应靠近蒸馏烧瓶的支管口处 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 焰色反应时,用稀硫酸洗净铂丝,并在火焰上灼烧至无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 钠和水反应:2Na+2H2O=2Na++2OH-+H2↑ | |
| B. | 盐酸与氢氧化钡溶液反应:H++OH-=H2O | |
| C. | 三氯化铁腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+ | |
| D. | 金属铝与氢氧化钠溶液反应:2Al+2OH-=2AlO2-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂是影响化学反应速率的本质因素 | |
| B. | 当反应体系容积不变时,减小反应物的量肯定能降低反应速率 | |
| C. | 可逆反应达到反应限度时,化学反应速率为0 | |
| D. | 化学反应速率可用单位时间内反应物的浓度变化量来表示 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com