
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子的电子层数多 | |
| C. | 1mol A从酸中置换H+生成的H2比1mol B从酸中置换H+生成的H2多 | |
| D. | 常温时,A能从水中置换出氢,而B不能 |
分析 金属的金属性越强,其最高价氧化物的水化物碱性越强,与酸或水反应越剧烈,较活泼金属能置换出较不活泼金属,据此分析解答.
解答 解:A.A原子的最外层电子数比B原子的最外层电子数少不能说明A的金属性大于B,如Ca的金属性大于Li,故A错误;
B.A原子的电子层数比B原子的电子层数多,不能说明A的金属性大于B,如Fe的金属性小于Na,故B错误;
C.1mol A从酸中置换H+生成的H2比1mol B从酸中置换H+生成的H2多,说明A失电子比B多,不能说明A的金属性大于B,故C错误;
D.常温下,A能从水中置换出氢,而B不能,说明A的活动性大于B,则A的金属性大于B,故D正确;
故选D.
点评 本题考查金属性强弱判断方法,可以利用其最高价氧化物的水化物碱性、金属之间的置换反应、金属与水或酸置换出氢气的难易程度来判断,金属性强弱与失电子难易程度有关,与失电子多少、电子层数多少无关,易错选项是BC.


科目:高中化学 来源: 题型:选择题
| 实验 | 实验目的 | |
| A | 乙醇、乙酸与浓硫酸混合共热一段时间,对混合液直接蒸馏 | 制备纯净的乙酸乙酯 |
| B | 将某气体通入品红溶液,溶液褪色 | 检验气体中的SO2 |
| C | 测定等物质的量浓度的HCOOK和K2S溶液的pH | 比较Ka(HCOOH)和Ka2(H2S)的大小 |
| D | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4和KMnO4溶液,观察气体产生的速度 | 比较CuSO4和KMnO4的催化效果 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
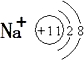 ;B与空气反应的化学方程式2NO+O2=2NO2.
;B与空气反应的化学方程式2NO+O2=2NO2.
 ;气体D的结构式
;气体D的结构式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
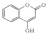 ,常用于制备抗凝血药,可通过下列流程合成:
,常用于制备抗凝血药,可通过下列流程合成: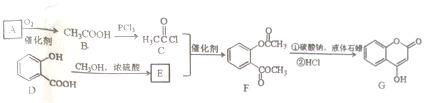
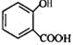 +CH3OH$?_{△}^{浓硫酸}$
+CH3OH$?_{△}^{浓硫酸}$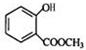 +H2O.
+H2O.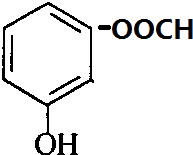 、
、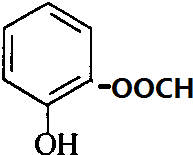 、
、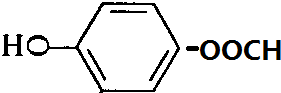 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O、CO2 | B. | MgF2、H2O2 | C. | NaOH、Ba(OH)2 | D. | NaCl、KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 | |
| B. | 生铁比软铁芯(几乎是纯铁)容易生锈 | |
| C. | 铁质器件附有铜质配件,接触处容易生铁锈 | |
| D. | 银质奖牌放置久了表面变暗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在离子晶体里,只存在离子键 | |
| B. | 共价化合物里,一定不存在离子键 | |
| C. | 非金属元素之间只能形成共价键 | |
| D. | 由不同种元素组成的多原子分子里,一定只有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
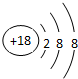 ;
; ①的气态氢化物的电子式:
①的气态氢化物的电子式: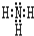 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com