
| A. | 铝制容器可以贮运浓硝酸 | B. | 甲醛可用作浸制标本 | ||
| C. | 碳酸氢钠可用来治疗胃酸过多 | D. | 明矾可用作消毒剂 |
分析 A.常温下浓硝酸和铝发生钝化现象;
B.甲醛可用于杀菌消毒;
C.碳酸氢钠能和稀盐酸反应生成氯化钠和水、二氧化碳;
D.明矾中铝离子水解生成氢氧化铝胶体而具有吸附性,但明矾没有强氧化性.
解答 解:A.常温下,浓硝酸和铝发生氧化还原反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以常温下铝制容器可以贮运浓硝酸,故A正确;
B.甲醛可使蛋白质变性,可用作防腐剂,浸制生物标本,故B正确;
C.胃酸的主要成分是盐酸,碳酸氢钠和稀盐酸反应生成氯化钠和二氧化碳、水,从而降低盐酸浓度,则碳酸氢钠可用来治疗胃酸过多,故C正确;
D.明矾中铝离子水解生成氢氧化铝胶体而具有吸附性,所以明矾能净水,但明矾没有强氧化性,所以不能杀菌消毒,故D错误;
故选D.
点评 本题考查物质用途,涉及钝化、蛋白质的性质、盐类水解等知识点,为高频考点,明确物质性质是解本题关键,注意蛋白质变性与盐析区别,题目难度不大.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 盐酸、苛性钠、偏铝酸钠 | B. | 硅酸、乙醇、小苏打 | ||
| C. | 硫酸、纯碱、硅酸钠 | D. | 碳酸、烧碱、一水合氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有$\frac{1}{2}$NA个硫原子被还原 | B. | 有$\frac{1}{3}$NA个氮原子被氧化 | ||
| C. | 有$\frac{3}{4}$NA个二氧化硫分子生成 | D. | 有$\frac{2}{3}$NA个硫酸铵分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 | |
| B. | 澄清的石灰水跟盐酸反应H++OH-═H2O | |
| C. | 碳酸钡溶于醋酸BaCO3+2H+═Ba2++H2O+CO2↑ | |
| D. | 金属钠跟水反应Na+H2O═Na ++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
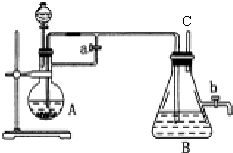
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
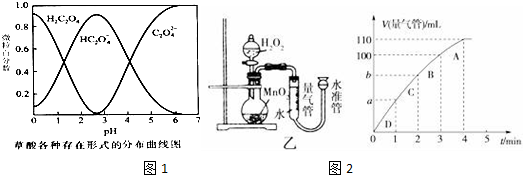
| 实验编号 | T/K | 催化剂的用量/g | 酸性KMnO4溶液的浓度/mol•L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b.实验①和③ 探究温度对反应速率的影响; c.实验①和④ 探究催化剂对反应速率的影响. |
| ② | ||||
| ③ | 0.010 | |||
| ④ |
| 实验编号 | 溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| Ⅰ | 14.0 | 13.0 | 11.0 |
| Ⅱ | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | H+ Na+ Al3+ Ag+ Ba2+ |
| 阴离子 | OH- Cl- CO32- NO3- SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com