
判断正误,正确的划“√”,错误的划“×”
(1)强氧化剂与强还原剂混合不一定能发生氧化还原反应 ( )
解析 强氧化剂与强还原剂发生反应需要一定的条件,如H2和O2发生反应需要点燃或 光照。
光照。
(2)阳离子只有氧化性,阴离子只有还原性 ( )
(3)元素的非金属性越强,其氧化性越强,相应单质越活泼 ( )
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:高中化学 来源: 题型:
X、Y两根金属棒插入Z溶液中构成下图的装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )
| 编号 | X | Y | Z |
| A | Zn | Cu | 稀硫酸 |
| B | Cu | Zn | 稀硫酸 |
| C | Cu | Ag | 硫酸铜溶液 |
| D | Ag | Zn | 硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机实验操作或叙述正确的是( )
A.乙酸乙酯中的少量乙酸可用浓的NaOH溶液除去
B.除去乙烷中少量的乙烯:酸性高锰酸钾溶液,气液分离
C.用热的纯碱溶液可洗去试管内壁上附着的油脂
D.制乙酸乙酯时,向试管中加入无水乙醇,然后边摇动试管边加入稀硫酸和冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化。已知:破坏1 mol氢气中的化学键需要吸收436 kJ能量;破坏1/2 mol氧气中的化学键需要吸收 249 kJ的能量;形成水分子中1 mol H—O键能够释放 463 kJ能量。下图表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上。
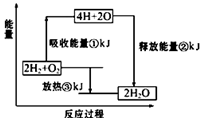
①________kJ ②________kJ ③________kJ
(2)今有2H2+O2 =2H2O反应构成燃料电池,则负极通的应是 ,用KOH溶液作电解质,负极的电极反应式为 ,正极的电极反应式为 。
(3)若把H2改为CH3OH,用KOH溶液作电解质,则负极的电极反应式: .
(4)电解原理在化学工业中有广泛的应用。右图表示一个电解池,电极材料为惰性电极,U形管装有饱和食盐水;实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中阴极上的电极反应式为______________________,在阴极附近观察到的现象是_______________。

②随着气体的生成,饱和食盐水中产生了两种不同的颜色:
阳极区是 色,阴极区是 色。
③电解一段时间后取出电极,将U形管内的液体搅拌混匀,又发生了化学反应,该反应的化学方程式是 ;该溶液可用作消毒剂,原因是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是
( )
A.CO2是氧化产物
B.H2C2O4在反应中被氧化
C.H2C2O4的氧化性强于ClO2的氧化性
D.ClO2作水处理剂时,利用了其强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关。下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与FeCl3溶液 ⑤Cl2和NaOH溶液 ⑥Fe和HNO3溶液 ⑦Fe和H2SO4溶液 ⑧Na和O2
(1)由于浓度不同而发生不同氧化还原反应的是________________________________。
(2)由于温度不同而发生不同氧化还原反应的是________________________________。
(3)氧化还原反应不受浓度、温度影响的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是 ( )
①维生素C具有还原性,在人体内起抗氧化作用 (2009·天津理综,1A)
②NO2溶于水时发生氧化还原反应 (2012·天津理综,2C)
③1 mol Cl2参加反应转移电子数一定为2NA (2010·福建理综,7C)
④阴离子都只有还原性 (2008·北京理综,8B)
⑤BaSO3和H2O2的反应为氧化还原反应
A.①②⑤ B.②③⑤ C.③④⑤ D.①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是________(填序号)。
A.Cl2 B.H2O2
C.ClO2 D.O3
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2===A+NH3↑,则生成物A的化学式为________,H2O2被称为“绿色氧化剂”的理由是________________________。
(3)漂白剂亚氯酸钠(NaClO2)在常温下、黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为HClO2―→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子数约为____________。
(4)“84”消毒液(主要成分是NaClO)和洁厕 剂(主要成分是浓盐酸)不能混用,原因是__________
剂(主要成分是浓盐酸)不能混用,原因是__________ ________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
________________________(用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)—空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%—30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是( )。
A.电池工作时,溶液中负极附近溶液的碱性增强,而电解质溶液pH减小
B.正极的电极反应式是:O2+4H++4e-=2H2O
C.负极的电极反应式是:N2H4+4OH――4e-=4H2O+N2↑ D.溶液中阴离子向正极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com