
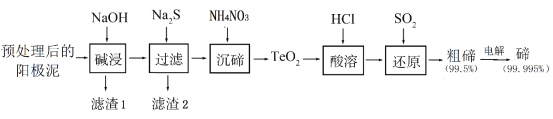
【题目】碲(Te)元素是当今新材料的主要成分之一。工业上从电解法精炼铜的阳极泥中提取纯度较高的碲,经预处理后的阳极泥中含TeO2及铁、铅、铜的化合物等,通过以下流程得到:
已知:①TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。
②部分难溶物的Ksp如表:
化合物 | Fe(OH)2 | Pb(OH)2 | Cu(OH)2 | FeS | PbS | CuS |
Ksp | 8×10-16 | 1.2×10-15 | 1.3×10-20 | 4×10-19 | 1×10-28 | 6×10-36 |
回答下列问题:
(1)“碱浸”时TeO2发生反应的化学方程式为___________。
(2)加入Na2S溶液的主要目的是___________。
(3)“沉碲”发生反应的化学方程式为_______。
(4)“酸溶”后,将SO2通入溶液中进行“还原”得到粗碲,该反应的化学方程式是___________。
(5)电解法提纯粗碲时,以Na2TeO3溶液为电解质溶液,阳极材料为___________。电解过程中阴极的电极反应式为___________。
(6)常温下,向0.lmol/LNa2TeO3溶液中滴加盐酸,当溶液pH=5时,溶液中c(TeO32-):c(H2TeO3)=___________。(已知:H2TeO3的Ka1=1.0×10-3Ka2=2.0×10-8)
【答案】TeO2+2NaOH=Na2TeO3+H2O 将溶液中的铁、铅、铜以更难溶的硫化物形式除去 Na2TeO3+2NH4NO3=2NaNO3+TeO2↓+2NH3+H2O 2SO2+TeCl4+4H2O=2H2SO4+Te+4HCl 粗碲 TeO32-+3H2O+4e-=Te+6OH- 0.2
【解析】
TeO2有两性,结合化合价可知,“碱浸”主要将TeO2转化为Na2TeO3;
“过滤”将未除去的Fe、Pb、Cu元素转化为更难溶的硫化物除去;
“沉碲”过程,从流程来看是将TeO32-转化为TeO2沉淀;
“酸溶”过程,TeO2转化为TeCl4;
“还原”过程,SO2将TeCl4还原为Te,得粗Te;
“电解”过程,粗Te作阳极,失电子,在阳极溶解,纯Te作阴极,阴极得电子,得到纯度更高的纯Te。
(1)TeO2有两性,结合化合价可知,“碱浸”时NaOH和TeO2反应生成为Na2TeO3和H2O,反应的化学方程式为TeO2+2NaOH=Na2TeO3+H2O,故答案为:TeO2+2NaOH=Na2TeO3+H2O;
(2)由分析可知,加入Na2S溶液的主要目的是将溶液中的铁、铅、铜以更难溶的硫化物形式除去,故答案为:将溶液中的铁、铅、铜以更难溶的硫化物形式除去;
(3)“沉碲”将TeO32-转化为TeO2沉淀,原因为TeO32-和NH4+发生双水解,反应的化学方程式为Na2TeO3+2NH4NO3=2NaNO3+TeO2↓+2NH3+H2O,故答案为:Na2TeO3+2NH4NO3=2NaNO3+TeO2↓+2NH3+H2O;
(4)“还原”过程,SO2将TeCl4还原为Te,得粗Te,结合得失电子守恒、原子守恒可得方程式为:2SO2+TeCl4+4H2O=2H2SO4+Te+4HCl,故答案为:2SO2+TeCl4+4H2O=2H2SO4+Te+4HCl;
(5)由分析可知,阳极材料为粗碲,以Na2TeO3溶液为电解质溶液,则阴极为TeO32-得电子生成Te,结合电荷守恒、原子守恒可得阴极的电极反应为:TeO32-+3H2O+4e-=Te+6OH-,故答案为:粗碲;TeO32-+3H2O+4e-=Te+6OH-;
(6)pH=5时,c(H+)=10-5mol/L。H2TeO3![]() H++HTeO3-,Ka1=
H++HTeO3-,Ka1=![]() =1.0×10-3,HTeO3-
=1.0×10-3,HTeO3-![]() H++TeO32-,Ka2=
H++TeO32-,Ka2=![]() =2.0×10-8,
=2.0×10-8,![]()
![]() ,所以,
,所以,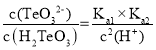
![]() =0.2,故答案为:0.2。
=0.2,故答案为:0.2。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中的浓硫酸滴入②中,预测的现象与结论相符的是( )

A. 若②为浓盐酸;产生大量气体产生;说明硫酸的酸性比盐酸强
B. 若②为铜片;有气泡产生,底部生成灰白色固体;说明浓硫酸有强氧化性
C. 若②为蓝色硫酸铜晶体;蓝色晶体变为白色;说明浓硫酸有吸水性,发生物理变化
D. 若②为蔗糖;白色固体变为黑色海绵状,有气体放出;说明浓硫酸有脱水性、氧化性
【答案】D
【解析】
A.浓硫酸具有吸水性,浓盐酸具有挥发性,浓硫酸吸收浓盐酸中的水分导致浓盐酸浓度增大而加强其挥发性,浓硫酸和盐酸都是强酸,该实验体现浓盐酸的挥发性和浓硫酸的吸水性,故A错误。
B.常温下浓硫酸和Cu不反应,所以没有明显现象,故B错误。
C.浓硫酸具有吸水性,能吸收五水硫酸铜中的结晶水而使五水硫酸铜变为无水硫酸铜,固体由蓝色变为白色,该实验为化学变化,故C错误。
D.浓硫酸能将有机物中的H、0元素以2:1水的形式脱去而体现脱水性,还能将蔗糖脱水后形成的碳单质. 氧化为二氧化碳.同时还生成刺激性气味的二氧化硫,体现了浓硫酸的强氧化性.故D正确。
答案选D。
【题型】单选题
【结束】
9
【题目】已知NH4NO3在空气中爆炸时的反应为4NH4NO3![]() 3N2↑+2NO2↑+8H2O↑。下列说法不正确的是( )
3N2↑+2NO2↑+8H2O↑。下列说法不正确的是( )
A.NH4NO3在高温下爆炸时可以看到红棕色的烟雾
B.NH4NO3的含氮量小于氯化铵
C.实验室不能用NH4NO3固体与Ca(OH)2固体混合加热制备NH3
D.乘坐火车时不能携带NH4NO3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制500mL 0.100 mol·Lˉ1的NaCl溶液,部分实验操作示意图如下:

下列说法正确的是
A. 实验中需用的仪器有:天平、250mL容量瓶、烧杯、玻璃棒、胶头滴管等
B. 上述实验操作步骤的正确顺序为①②④③
C. 容量瓶需要用自来水、蒸馏水洗涤,干燥后才可用
D. 定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2﹣羟基异丁酸乙酯能溶于水,是一种应用于有机合成和药物制造的化工原料。

(1)2﹣羟基异丁酸乙酯的分子式为_________,不同化学环境的氢在核磁共振氢谱图中有不同的吸收峰,则2﹣羟基异丁酸乙酯有_________个吸收峰;
(2)①②的反应类型分别为_________,_________;
(3)已知I为溴代烃,I→B的化学方程式为_________;
(4)缩聚产物F的结构简式为_________;
(5)下列关于![]() 和
和 的说法正确的有_________(双选,填字母);
的说法正确的有_________(双选,填字母);
A.后者遇到FeCl3溶液显紫色,而前者不可
B.两者都可以与NaHCO3溶液反应放出CO2
C.两者都可以与氢氧化钠溶液发生反应,当两者物质的量相等时,消耗氢氧化钠的量不相等
D.两者都可以与氢气发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO3—的摩尔电导率分别为0.60、1.98、0.45,据此可判断,向饱和的澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是( )
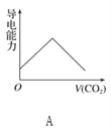
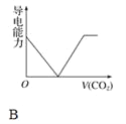

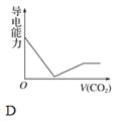
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
A. 1 L 1 mol/L的Na2CO3溶液中含有的CO32-数目为![]()
B. 常温常压下,8 g O2含有的电子数是4NA
C. 标准状况下,2.24 L CCl4中含有的分子数为0.1NA
D. 25℃时,1 L pH=13的 Ba(OH)2溶液中含有的OH-数目为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应能用离子方程式2H+ + CO32-=CO2↑ + H2O表示的是
A.HCl溶液与MgCO3反应
B.CH3COOH与K2CO3溶液反应
C.HNO3溶液与NaHCO3溶液反应
D.H2SO4溶液与(NH4)2CO3溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雌二醇的结构简式如图,下列说法不正确的是
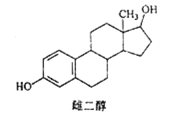
A. 能与 Na、NaOH溶液、Na2CO3溶液反应
B. 能发生加成反应、取代反应、消去反应
C. 该分子中所有碳原子不可能在同一个平面内
D. 可与 FeC13溶液发生显色反应,但不能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )

A. M和N互为同分异构体
B. M分子中所有碳原子均处于同一平面上
C. N与 属于同系物
属于同系物
D. M和N均能使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com