
【题目】氯化钠晶体熔化的过程中,破坏了( )
A.离子键和金属键B.离子键
C.共价键和金属键D.共价键
科目:高中化学 来源: 题型:
【题目】不锈钢表面用硝酸和氢氟酸的混酸处理后,产生的酸洗废液中含有Fe3+、Ni2+、NO3﹣、F﹣和+6价铬的含氧酸根离子等.如图是综合利用该酸洗废液的工艺流程: 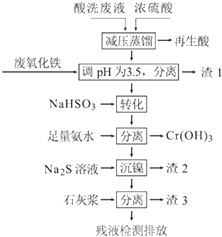
已知:
①金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
②Ni2+与足量氨水的反应为:Ni2++6NH3[Ni(NH3)6]2+
(1)再生酸中含有 , 采取减压蒸馏的原因是 .
(2)利用废氧化铁(主要成分为Fe2O3)代替烧碱调节pH的好处是 .
(3)请写出“转化”时NaHSO3与Cr2O72﹣发生反应的离子反应方程式: .
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为: .
(5)滤渣3的主要成分为CaF2、Ca(OH)2和 .
(6)经检测,最后的残液中c(Ca2+)=0.004molL﹣1 , 则残液中F﹣浓度为mgL﹣1 , (填“符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10﹣11 mol3L﹣3 , 国家排放标准要求氟离子浓度小于10mgL﹣1].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙醛是无色易流动液体,有刺激性气味。熔点-121℃,沸点 20.8℃,相对密度小于 1,可与水和乙醇等一些有机物质互溶。要从水与乙醛的混合物中将乙醛分离出来,应选用( )
A. 蒸馏 B. 分液 C. 过滤 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合题。
(1)在一定条件下,21.6gA单质与1.20molCl2完全反应,生成0.800molAClx,则x= , A的摩尔质量为 .
(2)实验室需要2.0molL﹣1NaOH溶液90mL,用托盘天平称取氢氧化钠,其质量为g;
(3)将5.60g铁投入100mL某浓度的盐酸中,铁和盐酸恰好完全反应.求:
①所用盐酸中HCl的物质的量浓度为
②反应中生成的H2在标准状况下的体积为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应A(g)+B(g)C(g)△H<0达到平衡后,据下列图象判断:
达到新的平衡对应的图象 | 平衡移动方向 | |
(i)使用催化剂 | ||
(ii)升温 | ||
(iii)降压 | ||
(iv)增加A的量 | ||
(v)减少C的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.现有右图所示裝置,为实现下列实验目的,其中应以a端作为入口的是__________。
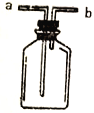
A.瓶内盛碱石灰,用以干燥气体
B.瓶内盛饱和食盐水,用以除去Cl2中混有的少量HCl
C.瓶内盛水,用以测量某难溶于水的气体体积
D.瓶内贮存气体,加水时气体可被排出
E.收集密度比空气大的气体
F.收集密度比空气小的气体
Ⅱ.欲用98%的浓硫酸(密度为1.84g·cm3)配制浓度为1mol/L的稀硫酸480mL。
(1)需取用浓硫酸的体积为______________mL(结果保留一位小数)
(2)下列情况中,会使所配溶液的浓度偏低的是__________。
A.将量筒中的浓硫酸转入烧杯后,用水洗涤量筒,将洗液也转入烧杯中
B.稀释浓硫酸后立即转入容量瓶
C.定容时加水不慎超过刻度线
D.定容时仰视刻度线
(3)容量瓶在使用前,首先应检查___________________。
(4)此实验中,玻璃棒的两个作用分别是_________、_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe2O3的混合物中加入100mL浓度为1.0mol·L-1的盐酸,恰好使混合物完全溶解,有气体放出,所得溶液中加入KSCN溶液后无红色出现。若用足量的CO在高温下还原相同质量此混合物,能得到铁的质量是( )
A. 11.2g B. 5.6g
C. 2.8g D. 1.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应。若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为( )
A. 1:2:3 B. 1:6:9 C. 1:3:3 D. 1:3:6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com