
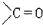 +RMgX”ś
+RMgX”ś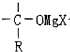
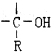

 £¬
£¬ £®
£® ·ÖĪö ĢžX·Ö×ÓŹ½ĪŖC4H8£¬ĒŅĪŖĮ“ד½į¹¹£¬ÓėHBr·“Ӧֻɜ³ÉŅ»ÖÖ²śĪļA£¬ŌņXĪŖCH3CH=CHCH3£¬CH3CH=CHCH3¾Ņ»ĻµĮŠ·“Ó¦Ö®ŗóÉś³ÉFÓ¦ĪŖ“¼£¬ŌņFŹĒ3£¬4-¶ž¼×»ł-3-¼ŗ“¼£¬F·¢ÉśĻūČ„·“Ӧɜ³ÉG£¬GŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉH£¬HŗĶĒāŃõ»ÆÄĘČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³ÉI£¬IŗĶĖį·¢Éśõ„»Æ·“Ӧɜ³ÉJ£¬ĖłŅŌGĪŖ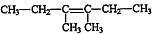 £¬HĪŖ
£¬HĪŖ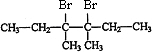 £¬IĪŖ
£¬IĪŖ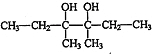 £¬FĪŖ
£¬FĪŖ £¬EĪŖ
£¬EĪŖ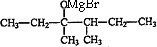 £¬DĪŖ
£¬DĪŖ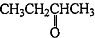 £¬CĪŖ
£¬CĪŖ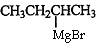 £¬BĪŖ
£¬BĪŖ £¬AĪŖ
£¬AĪŖ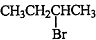 £¬IŗĶ¶žŌŖĖį·¢Éśõ„»Æ·“Ӧɜ³ÉJ£¬C10H16O4µÄ¾ßÓŠĮłŌŖ»·µÄĪļÖŹJ£¬ŌņJµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬IŗĶ¶žŌŖĖį·¢Éśõ„»Æ·“Ӧɜ³ÉJ£¬C10H16O4µÄ¾ßÓŠĮłŌŖ»·µÄĪļÖŹJ£¬ŌņJµÄ½į¹¹¼ņŹ½ĪŖ£ŗ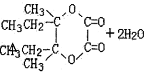 £¬½įŗĻÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹŅŌ¼°ĢāÄæŅŖĒóæɽā“šøĆĢā£®
£¬½įŗĻÓŠ»śĪļµÄ½į¹¹ŗĶŠŌÖŹŅŌ¼°ĢāÄæŅŖĒóæɽā“šøĆĢā£®
½ā“š ½ā£ŗĢžX·Ö×ÓŹ½ĪŖC4H8£¬ĒŅĪŖĮ“ד½į¹¹£¬ÓėHBr·“Ӧֻɜ³ÉŅ»ÖÖ²śĪļA£¬ŌņXĪŖCH3CH=CHCH3£¬CH3CH=CHCH3¾Ņ»ĻµĮŠ·“Ó¦Ö®ŗóÉś³ÉFÓ¦ĪŖ“¼£¬ŌņFŹĒ3£¬4-¶ž¼×»ł-3-¼ŗ“¼£¬F·¢ÉśĻūČ„·“Ӧɜ³ÉG£¬GŗĶäå·¢Éś¼Ó³É·“Ӧɜ³ÉH£¬HŗĶĒāŃõ»ÆÄĘČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³ÉI£¬IŗĶĖį·¢Éśõ„»Æ·“Ӧɜ³ÉJ£¬ĖłŅŌGĪŖ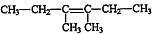 £¬HĪŖ
£¬HĪŖ £¬IĪŖ
£¬IĪŖ £¬FĪŖ
£¬FĪŖ £¬EĪŖ
£¬EĪŖ £¬DĪŖ
£¬DĪŖ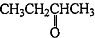 £¬CĪŖ
£¬CĪŖ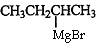 £¬BĪŖ
£¬BĪŖ £¬AĪŖ
£¬AĪŖ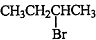 £¬IŗĶ¶žŌŖĖį·¢Éśõ„»Æ·“Ӧɜ³ÉJ£¬C10H16O4µÄ¾ßÓŠĮłŌŖ»·µÄĪļÖŹJ£¬ŌņJµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬IŗĶ¶žŌŖĖį·¢Éśõ„»Æ·“Ӧɜ³ÉJ£¬C10H16O4µÄ¾ßÓŠĮłŌŖ»·µÄĪļÖŹJ£¬ŌņJµÄ½į¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
£Ø1£©ĶعżŅŌÉĻ·ÖĪöÖŖ£¬XµÄ½į¹¹¼ņŹ½ŹĒ CH3CH=CHCH3£¬
¹Ź“š°øĪŖ£ŗCH3CH=CHCH3£»
£Ø2£©FĪŖ £¬FĆū³ĘĪŖ3£¬4-¶ž¼×»ł-3-¼ŗ“¼£¬FµÄĶ¬·ÖŅģ¹¹Ģåŗܶą£¬Āś×ćÖ÷Į“5øöĢ¼Ō×ÓĒŅ·Ö×ÓÖŠŗ¬Īåøö¼×»łµÄ“¼ĄąĶ¬·ÖŅģ¹¹ĢåÓŠCH3CH£ØCH3£©CH£ØCH3£©C£ØOH£©£ØCH3£©CH3”¢CH3CH£ØCH3£©C£ØOH£©£ØCH3£©CH£ØCH3£©CH3”¢£ØCH3£©2C£ØOH£©CH2C£ØCH3£©3”¢£ØCH3£©2CHCH£ØOH£©C£ØCH3£©3”¢CH3CH2C£ØCH3£©£ØOH£©C£ØCH3£©3”¢CH3CH£ØOH£©CH£ØCH3£©C£ØCH3£©3”¢£ØCH3£©2C£ØOH£©C£ØCH3£©2CH2H3”¢£ØCH3£©2CHC£ØCH3£©2CH£ØOH£©H3£¬¹²8 ÖÖ£¬
£¬FĆū³ĘĪŖ3£¬4-¶ž¼×»ł-3-¼ŗ“¼£¬FµÄĶ¬·ÖŅģ¹¹Ģåŗܶą£¬Āś×ćÖ÷Į“5øöĢ¼Ō×ÓĒŅ·Ö×ÓÖŠŗ¬Īåøö¼×»łµÄ“¼ĄąĶ¬·ÖŅģ¹¹ĢåÓŠCH3CH£ØCH3£©CH£ØCH3£©C£ØOH£©£ØCH3£©CH3”¢CH3CH£ØCH3£©C£ØOH£©£ØCH3£©CH£ØCH3£©CH3”¢£ØCH3£©2C£ØOH£©CH2C£ØCH3£©3”¢£ØCH3£©2CHCH£ØOH£©C£ØCH3£©3”¢CH3CH2C£ØCH3£©£ØOH£©C£ØCH3£©3”¢CH3CH£ØOH£©CH£ØCH3£©C£ØCH3£©3”¢£ØCH3£©2C£ØOH£©C£ØCH3£©2CH2H3”¢£ØCH3£©2CHC£ØCH3£©2CH£ØOH£©H3£¬¹²8 ÖÖ£¬
¹Ź“š°øĪŖ£ŗ3£¬4-¶ž¼×»ł-3-¼ŗ“¼£»8£»
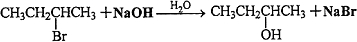
£Ø3£©AĪŖ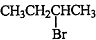 £¬ŌŚ¼īŠŌĢõ¼žĻĀĖ®½ā£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ
£¬ŌŚ¼īŠŌĢõ¼žĻĀĖ®½ā£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©øł¾ŻJµÄ·Ö×ÓŹ½æÉÖŖ¶žŌŖĖįĪŖŅŅ¶žĖį£¬·“Ó¦µÄ·½³ĢŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬ĢāÄæÄŃ¶Č½Ļ“󣬱¾Ģā×¢Ņā½įŗĻĢāøųŠÅĻ¢ŅŌFĪŖ½ā“šøĆĢāµÄĶ»ĘĘæŚ£¬ÓĆÄęĶʵķ½·Ø½ųŠŠĶʶĻ£¬“šĢāŹ±×¢Ņā°ŃĪÕ·“Ó¦Ģõ¼ž£¬½čŅŌĶʶĻ¹ŁÄÜĶŵıä»Æ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĀČ»ÆĒāµÄµē×ÓŹ½£ŗ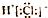 | |
| B£® | ŅŅĶéµÄ½į¹¹¼ņŹ½£ŗC2H6 | |
| C£® | ĀĮµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼£ŗ | |
| D£® | ĮņĖįÄʵĵēĄė·½³ĢŹ½£ŗNa2SO4=2Na++$S{{O}_{4}}^{2-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ÖŠ¹śÕžø®³ŠÅµ£¬µ½2020Äź£¬µ„Ī»GDP¶žŃõ»ÆĢ¼ÅŷűČ2005ÄźĻĀ½µ40%”«50%£®
ÖŠ¹śÕžø®³ŠÅµ£¬µ½2020Äź£¬µ„Ī»GDP¶žŃõ»ÆĢ¼ÅŷűČ2005ÄźĻĀ½µ40%”«50%£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 PETŹĒ¾Ūõ„ĄąŗĻ³É²ÄĮĻ£¬ŅŌĀ±“śĢžĪŖŌĮĻŗĻ³ÉPETµÄĻßĀ·ČēĶ¼£Ø·“Ó¦ÖŠ²æ·ÖĪŽ»ś·“Ó¦Īļ¼°²śĪļŅŃŹ”ĀŌ£©£®ŅŃÖŖRX2ŹĒ·¼Ļć×å»ÆŗĻĪļ£ØR”¢R”ä“ś±ķĢž»ł£¬X“ś±ķĀ±ĖŲŌ×Ó£©£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ175£¬ĘäÖŠXŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ40.6%£®
PETŹĒ¾Ūõ„ĄąŗĻ³É²ÄĮĻ£¬ŅŌĀ±“śĢžĪŖŌĮĻŗĻ³ÉPETµÄĻßĀ·ČēĶ¼£Ø·“Ó¦ÖŠ²æ·ÖĪŽ»ś·“Ó¦Īļ¼°²śĪļŅŃŹ”ĀŌ£©£®ŅŃÖŖRX2ŹĒ·¼Ļć×å»ÆŗĻĪļ£ØR”¢R”ä“ś±ķĢž»ł£¬X“ś±ķĀ±ĖŲŌ×Ó£©£¬Ļą¶Ō·Ö×ÓÖŹĮæĪŖ175£¬ĘäÖŠXŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ40.6%£® £®
£® +nHOCH2CH2OH$\stackrel{Ņ»¶ØĢõ¼žĻĀ}{”ś}$
+nHOCH2CH2OH$\stackrel{Ņ»¶ØĢõ¼žĻĀ}{”ś}$ +2nH2O£®
+2nH2O£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


 £®
£® £®
£® £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H£¼0±ķŹ¾·ÅČČ·“Ó¦£¬”÷H£¾0±ķŹ¾ĪüČČ·“Ó¦ | |
| B£® | Čē¹ū·“Ó¦ĪļĖł¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚÉś³ÉĪļĖł¾ßÓŠµÄ×ÜÄÜĮ棬Ōņ·¢ÉśµÄ·“Ó¦ŹĒ·ÅČČ·“Ó¦ | |
| C£® | ŌŚĻ”ČÜŅŗÖŠ1molĖįŗĶ1mol¼īĶźČ«·“Ó¦Ėł·Å³öµÄČČĮ棬½Š×öÖŠŗĶČČ | |
| D£® | 1 mol H2Óė0.5 mol O2·“Ó¦·Å³öµÄČČ¾ĶŹĒH2µÄČ¼ÉÕČČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com