
| A.氯碱工业中隔离两电极的材料是阳离子交换膜,因此该生产方法又称“阳离子交换膜法” |
| B.生产普通玻璃的主要原料及设备:石灰石、石英、纯碱及玻璃熔炉 |
| C.由于常压下SO2转化为SO3的转化率很高,所以SO2接触氧化时不采用高压的反应条件 |
| D.合成氨的反应是放热反应,因此工业合成常采用低温条件 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
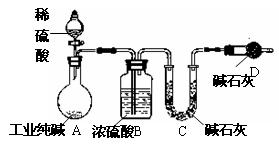
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
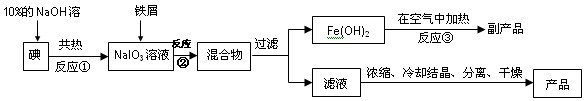
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
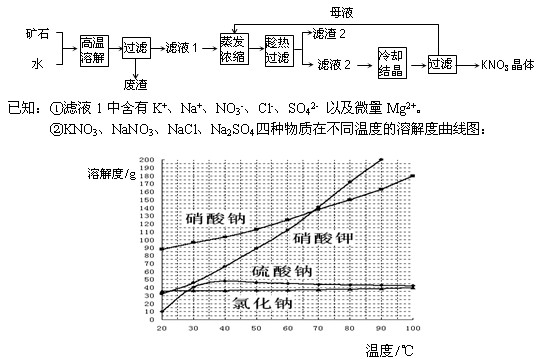
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 是一种重要的化工原料,工业上生产硝酸的主要过程如下:
是一种重要的化工原料,工业上生产硝酸的主要过程如下: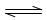 2NH3(g) △H<0
2NH3(g) △H<0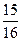 ,则N2的转化率a1= ;
,则N2的转化率a1= ;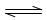 2NO2(g)△H>0
2NO2(g)△H>0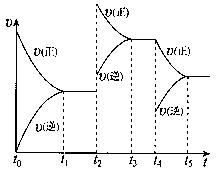
 2将NO2还原为N2。
2将NO2还原为N2。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
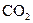 含量高的水浇灌农作物有许多优点,下列对其优点的分析不正确的是( )
含量高的水浇灌农作物有许多优点,下列对其优点的分析不正确的是( )| A.加速农作物的光合作用 |
| B.有利土壤中Ca、Mg元素被农作物吸收 |
| C.改良碱性土壤 |
| D.增加土壤中N、P元素含量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2SO4·1/9H2O |
| B.SO3·10/9H2O |
| C.H2SO4·SO3 |
| D.SO3·H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③ | B.①② | C.①③ | D.①②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) ,在反应过程中,
2NH3(g) ,在反应过程中, t1、t2、t3、t4时条件改变,正反应速率发生变化,如右图,对于可能的条件改变下列判断正确的是
t1、t2、t3、t4时条件改变,正反应速率发生变化,如右图,对于可能的条件改变下列判断正确的是
A.t1时可能升高了温度 | B.t2时可能使用了催化剂 |
C.t3时可能减小了压强 | D.t4时可能降低了温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com