
| A. | 含有AgCl和AgI固体的悬浊液:c(Ag+)>c(C1-)=c(I-) | |
| B. | CO2的水溶液:c(H+)>c(HCO3-)═2c(CO32-) | |
| C. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) | |
| D. | 含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)═2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
分析 A.AgCl和AgI固体的悬浊液中氯化银溶解度大于碘化银;
B.二氧化碳的水溶液中碳酸分步电离,第二步电离微弱;
C.NaHSO4溶液中存在质子守恒分析,硫酸氢钠电离出钠离子、氢离子、硫酸根离子,溶液中质子守恒分析;
D.依据溶液中元素物料守恒计算,2n(Na)=3n(C2O42-)
解答 解:A.AgCl和AgI固体的悬浊液中氯化银溶解度大于碘化银,c(Ag+)>c(Cl-)>c(I-),故A错误;
B.二氧化碳的水溶液中碳酸分步电离,第二步电离微弱,H2CO3?H++HCO3-,HCO3-?H++CO32-,c(H+)>c(HCO3-)>2c(CO32-),故B错误;
C.NaHSO4溶液中存在质子守恒分析,硫酸氢钠电离出钠离子、氢离子、硫酸根离子,NaHSO4 =Na++H++SO42-,H2O?H++OH-,溶液中质子守恒,c(H+)=c(SO42-)+c(OH-),故C正确;
D.依据溶液中元素物料守恒计算,含等物质的量NaHC2O4和Na2C2O4的溶液:2c(Na+)=3[c(HC2O4-)+C(C2O42-)+c(H2C2O4)],故D错误;
故选C.
点评 本题考查了电解质溶液中电离平衡分析,沉淀溶解平衡的理解应用,电解质溶液中物料守恒,质子守恒的分析判断,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:解答题
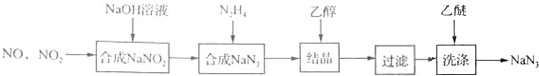
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入盐酸以除去硫酸钠中少量的碳酸钠杂质 | |
| B. | 用玻璃棒搅拌漏斗中的液体以加快反应速率 | |
| C. | 用稀硫酸和锌反应制氢气时加入少许硫酸铜以加快反应速率 | |
| D. | 在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称量时,将NaOH固体放在左盘内的纸上,称得质量为10.2 g | |
| B. | 用25 mL碱式滴定管量取高锰酸钾溶液,体积为16.60 mL | |
| C. | 用广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10 mL量筒量取NaCl溶液,体积为9.2 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13.8gNO2与足量水反应,转移电子敬目为0.2NA | |
| B. | 标准状况下,22.4L溴苯中含有氢原子数目为5NA | |
| C. | 500mL2mol/LNH4NO3溶液中,含有NH4+数目为NA | |
| D. | 用惰性电极电解足量CuSO4溶液,生成22.4L气体时转移电子数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 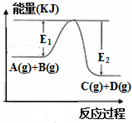 表示反应A(g)+B(g)→C(g)+D(g)是吸热反应,吸收能量(E2-E1)kJ | |
| B. |  为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1 | |
| C. | 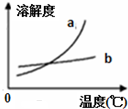 是物质a、b的溶解度曲线,可以用重结晶法从a、b混合物中提纯a | |
| D. | 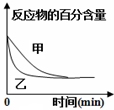 可表示压强对反应2A(g)+B(g)?3C(g)+D(s)的影响,且乙的压强大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液态HCl不导电,所以HCl不是电解质 | |
| B. | NH3溶于水形成的溶液能导电,所以NH3是电解质 | |
| C. | Cl2溶于水能导电,所以Cl2是电解质 | |
| D. | BaSO4在水溶液中难导电,但熔融下能导电所以BaSO4是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向50 mL 1 mol•L-1的盐酸中加入烧碱,水的KW不变 | |
| B. | NH4Cl和NH3•H2O混合液中,二者对对方的平衡都起了抑制作用 | |
| C. | 有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+) | |
| D. | 常温下0.1mol•L-1的HA溶液中c(OH-)/c(H+)=10-8,则0.01 mol•L-1HA溶液中c(H+)=1×10-4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com