

���� ��1��N��As��Ϊ��VA��Ԫ�أ��ǽ�����N��As��
��2������������ԭ��Ӧ����AsO43-�������Ӻ�ˮ��
��3������Asʧȥ���ӣ��������������ӣ�
��4��As2O5�ֽ�ΪAs2O3��Ҫ���յ�����Ϊ-619kJ/mol-��-914.6kJ/mol��=+295.4 kJ•mol-1���Դ���д�Ȼ�ѧ����ʽ��a�㷢��5As2O5$\frac{\underline{\;\;��\;\;}}{\;}$2As2O5•3As2O3+3O2�����Դ˼��㣮
��� �⣺��1��N��As��Ϊ��VA��Ԫ�أ��ǽ�����N��As����As����̬�⻯����ȶ��Ա�NH3 �����ʴ�Ϊ��VA������
��2������������ԭ��Ӧ����AsO43-�������Ӻ�ˮ�����ӷ�ӦΪAsO33-+I2+2OH-?AsO43-+2I-+H2O���ʴ�Ϊ��AsO33-+I2+2OH-?AsO43-+2I-+H2O��
��3������Asʧȥ���ӣ��缫��ӦΪAsO33-+H2O-2e-=AsO43-+2H+����������������AsO43-+2H++2e-=AsO33-+H2O��������pH����
�ʴ�Ϊ��AsO33-+H2O-2e-=AsO43-+2H+������
��4����ͼ���֪��As2O5�ֽ�ΪAs2O3��Ҫ���յ�����Ϊ-619kJ/mol-��-914.6kJ/mol��=+295.4 kJ•mol-1�����Ȼ�ѧ����ʽAs2O5��s��=As2O3��s��+O2��g����H=+295.4 kJ•mol-1��
a�㷢��5As2O5$\frac{\underline{\;\;��\;\;}}{\;}$2As2O5•3As2O3+3O2������a����Ʒʧ����w%=$\frac{3��32}{5����75��2+16��5��}$��100%=8.35��
�ʴ�Ϊ��As2O5��s��=As2O3��s��+O2��g����H=+295.4 kJ•mol-1��8.35��
���� ���⿼����ۺϣ��漰���ʺ������㡢�Ȼ�ѧ��Ӧ�����ȣ�Ϊ��Ƶ���㣬���շ�Ӧԭ����ͼ����ϢӦ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���


 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
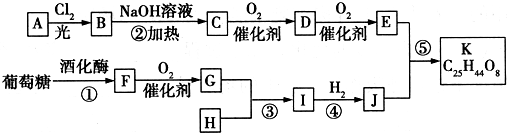
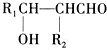
 ��G��CH3CHO��
��G��CH3CHO��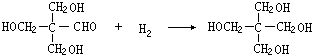 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
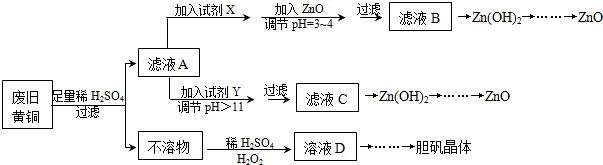
| Fe3+ | Fe2+ | Zn2+ | |
| ��ʼ������pH | 1.1 | 5.8 | 5.9 |
| ������ȫ��pH | 3.0 | 8.8 | 8.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ʵ�飺����KMnO4��Һ�г������ݣ�����ɫ����ȥ | |
| B�� |  ʵ�飺�ձ���Na2SiO3��Һ����ǣ���֤���ǽ�����C��Si | |
| C�� |  ʵЦ��ϡHN02��Ƭ�̣���Һ�������ݲ��������ƿ��ʼ�ձ�����ɫ | |
| D�� |  ʵ���ø�ʵ�װ�ÿ�֤�������ԣ�Cl2��Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
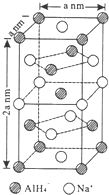 �⻯���ƣ�NaAlH4����һ���������ʴ�����ϣ���������Ti��NaAlH4��150��ʱ���⣬��170�桢15.2MPa���������ظ����⣮NaAlH4����AlCl3��NaH���ʵ������ºϳɣ�NaAlH4�ľ����ṹ��ͼ��ʾ����
�⻯���ƣ�NaAlH4����һ���������ʴ�����ϣ���������Ti��NaAlH4��150��ʱ���⣬��170�桢15.2MPa���������ظ����⣮NaAlH4����AlCl3��NaH���ʵ������ºϳɣ�NaAlH4�ľ����ṹ��ͼ��ʾ���� ����
����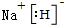 ����
���� �������������
��������λ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��һ���������������� | |
| B�� | ����NaHCO3��Ӧ��X��3�� | |
| C�� | X��ijЩͬ���칹��֮����ܷ���ȡ����Ӧ | |
| D�� | ����NaOH��Һ��Ӧ��X��������ͬ�Ĺ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
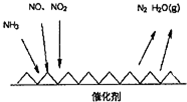
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | �������� | C�� | ������������ | D�� | ���Ȼ���ϡ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com