
 (1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH. 请回答下列问题:
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH. 请回答下列问题:分析 (1)①放电时,该电池是原电池,原电池负极上失电子化合价升高而发生氧化反应;
②放电时,正极上得电子发生还原反应,总反应方程式减去负极电极反应式即得正极反应式;
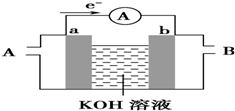
(2)①碱性条件下,电子由a流向b,则a为负极,b为正极,a电极上为甲烷失电子生成碳酸根离子;b电极上为氧气得电子生成氢氧根离子;
②根据负极上的反应,消耗负极质量减少一样多时,转移得电子的物质的量即可.
解答 解:(1)①电池的负极上发生氧化反应,正极上发生还原反应.由高铁电池放电时总反应方程式可知,负极材料应为作还原剂的Zn,故答案为:锌;
②正极上得电子发生还原反应,由电池的总反应方程式-负极反应式=正极反应式可知,正极反应式为FeO42-+3e-+4H2O═Fe(OH)3+5OH-,
故答案为:还原;FeO42-+3e-+4H2O═Fe(OH)3+5OH-;
(2)①碱性条件下,电子由a流向b,则a为负极,b为正极,a电极上为甲烷失电子生成碳酸根离子,其电极反应式为:CH4+10OH--8e-═CO32-+7H2O;
b电极上为氧气得电子生成氢氧根离子,其电极反应式为:2O2+4H2O+8e-═8OH-;
故答案为:CH4+10OH--8e-═CO32-+7H2O;2O2+4H2O+8e-═8OH-;
②根据负极上的电极反应式:CH4+10OH--8e-═CO32-+7H2O,铅蓄电池的负极上发生的反应为:Pb-2e-+SO42-=PbSO4,
所以当两种电池提供相同电量时,负极所消耗物质的物质的量之比为:1:4,故答案为:1:4.
点评 本题考查了原电池原理等知识,明确正负极上得失电子及反应类型是解本题关键,难点是电极反应式的书写.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.0 g氟化氢所含电子数为0.1NA | |
| B. | 1 mol Na2O2 跟足量H2O反应时得到电子的数目为2NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 核外电子排布相同的微粒化学性质也相同 | |
| C. | Cl?、S2?、Ca2+、K+半径逐渐减小 | |
| D. | 35Cl2与37Cl2得电子能力相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
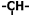 ),并且乙烯基和次甲基之间必须通过亚甲基相连,当该烃含有单环结构是分子中的乙烯基和亚甲基的个数依次为( )
),并且乙烯基和次甲基之间必须通过亚甲基相连,当该烃含有单环结构是分子中的乙烯基和亚甲基的个数依次为( )| A. | 2个,3个 | B. | 5个,3个 | C. | 4个,6个 | D. | 3个,6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②③ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com