
室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是( )
A.向0.10mol·L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-)
B.0.10mol·L-1CH3COONa溶液中通入HCl:c(Na+)>c(Cl-)>c(CH3COOH)
C.0.10mol·L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
D.向0.10mol·L-1NaHSO3溶液中通入NH3:c(Na+)>c(SO32-)>c(NH4+)
科目:高中化学 来源:2015-2016学年山西省高一下期中化学试卷(解析版) 题型:选择题
下列反应既能属于氧化还原反应,又属于吸热反应的是
A.铝片与稀盐酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应
D.硫在氧气中的燃烧反应
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市等十校高三3月联考理综化学试卷(解析版) 题型:选择题
常温下 0.1mol/L的H2A溶液中H2A、HA-、A2- 三者中所占物质的量分数(分布系数)随pH变化的关系如图所示。下列表述不正确的是( )
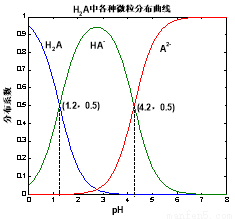
A.H2A 2H+ + A2- K=10-5.4
2H+ + A2- K=10-5.4
B.在 0.1mol/L NaHA 溶液中,各离子浓度大小关系为:
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.已知25℃时HF的 Ka=10-3.45,将少量H2A的溶液加入足量NaF溶液中,发生的反应为: H2A+F-═ HF+HA-
D.将等物质的量的NaHA、Na2A溶于水中,所得溶液pH恰好为4.2
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第六次适应性考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.一定条件下,将1 mol N2和3 mol H2混合发生反应,转移的电子总数为6 NA
B.1 L 0.1 mol·L-1的Na2CO3溶液中阴离子的总数大于0.1 NA
C.向FeI2溶液中通入适量Cl2,当有2 mol Fe2+被氧化时,消耗Cl2的分子数为NA
D.1 mol-CH3中所含的电子总数为10 NA
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三第八次模拟理综化学试卷(解析版) 题型:填空题
氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)氢气是清洁能源,其燃烧产物为__________。
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2,且反应前后B的化合价不变,该反应的化学方程式为 _,反应消耗1mol NaBH4时转移的电子数目为__________。
(3)储氢还可借助有机物,如利用环己烷和苯之间的可逆反应来实现脱氢和加氢:
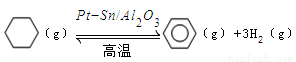 。
。
某温度下,向恒容密闭容器中加入环己烷,起始浓度为a mol/L,平衡时苯的浓度为bmol/L,该反应的平衡常数K= 。
(4)一定条件下,图示装置可实现有机物的电化学储氢(忽略其它有机物)。
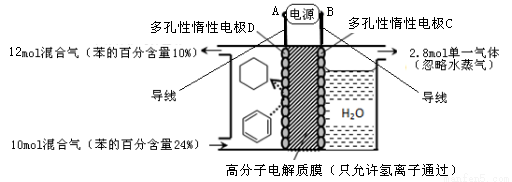
①导线中电子移动方向为 → 。(用A、B、C、D填空)
②生成目标产物的电极反应式为 。
③该储氢装置的电流效率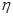 = 。(
= 。(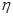 =
= ,计算结果保留小数点后1位)
,计算结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三第二次模拟理综化学试卷(解析版) 题型:实验题
【化学——选修2:化学与技术】
硝酸铵可用作化肥、军用炸药、杀虫剂、冷冻剂等,工业制取硝酸铵的工艺流程如下:
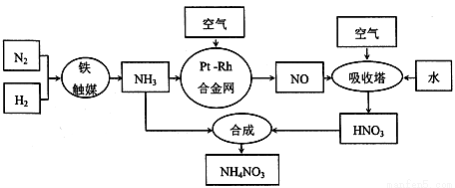
(l)合成氨气的工业设备名称是__________,设备中设置热交换器的目的是_______________,合成氨的原料气必须先脱硫,目的是_________________________________;
(2)吸收塔中反应的化学方程式为___________________,从生产流程看,吸收塔中需要补充空气,其原因是__________________________;
(3)生产硝酸的过程中常会产生氮的氧化物,可用如下三种方法处理:
方法一:碱性溶液吸收法
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+Na2CO3=NaNO2+NaNO3+CO2
方法二:NH3还原法
8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) △H =-2635 kJ/mol(NO也有类似的反应)
方法三:甲烷吸收法
CH4(g)+2NO2=CO2(g)+N2+2H2O(g) △H=+867 kJ/mol(NO也有类似的反应)
上述三种方法中,方法一的主要缺点是_______________________________;
方法三和方法二相比,方法三的缺点是_________________________;
(4)工业上也可以通过电解NO制备NH4NO3,其工作原理如下图所示。
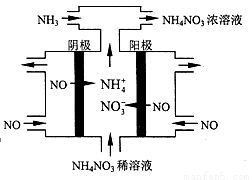
①图中通入NH3的目的是_____________;
②若维持电流强度为3A,电解2小时,理论上可制得NH4NO3的最大质量为_________g;
(已知F=96500 C·mol-l)(保留2位有效数字)。
(5)某化肥厂用NH3制备NH4NO3。己知:NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其他损耗)的百分比为______。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三第二次模拟理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z所处的族序数是周期序数的2倍。下列判断不正确的是
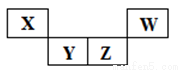
A.最高正化合价:X<Y<Z
B.原子半径:X<Y<Z
C.气态氢化物的热稳定性:Z<W
D.最高价氧化物对应水化物的酸性:X<Z
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏六盘山高中高一下期中化学试卷(解析版) 题型:填空题
某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为
(2)Fe2O3是主氧化剂,与Na反应生成的还原产物为 (已知该反应为置换反应).
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O,KClO4含有化学键的类型为 ,KCl在灼烧时得焰色为 色。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为 。
(5)100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况)。
①用碱石灰除去的物质为 ;
②该产气药剂中NaN3的质量分数为 。(4分)
查看答案和解析>>
科目:高中化学 来源:2016届海南海南中学高三考前模拟十一化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z的原子序数依次递增,X与Y、Z位于相邻周期,X形成的常见含氧酸能氧化氢后金属,Y、Z原子最外层电子数之比为3:7,下列说法正确的是
A.X的常见氢化物水溶液显弱碱性
B.组成为HZO的物质结构式为H—Z—O
C.最高价氧化物对应水化物酸性:Z>X>Y
D.简单离子半径:Z>Y>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com