
| 实验序号 | 待测液体积(mL) | 所消耗NaOH标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.54 |
| 2 | 20.00 | 6.00 | 26.00 |
| 3 | 20.00 | 1.40 | 21.36 |


科目:高中化学 来源:不详 题型:单选题
| A.Q1+Q2+Q3 |
| B.1.5Q1-0.5Q2+0.5Q3 |
| C.0.5Q1-1.5Q2+0.5Q3 |
| D.0.5(Q1+Q2+Q3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
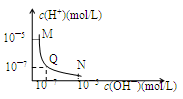
| A.M点所示溶液的导电能力强于Q点 |
| B.N点所示溶液中c(CH3COO―)>c(Na+) |
| C.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
| D.M点和N点所示溶液中H2O的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用标准NaOH溶液滴定盐酸溶液以测定其浓度:酚酞试液——浅红色 |
| B.用标准FeCl3溶液滴定KI以测定其浓度:淀粉溶液——蓝色 |
| C.用标准酸性KMnO4溶液滴定Na2SO3溶液以测定其浓度:KMnO4溶液——紫红色 |
| D.利用“Ag++SCN-=AgSCN↓”原理,用标准KSCN溶液滴定AgNO3溶液以测定其浓度:FeCl3溶液——红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同浓度的CH3COOH和NaOH溶液等体积混合 |
| B.pH=2的HCl和pH=12的NaOH溶液等体积混合 |
| C.pH=3的HCl和pH=12的NaOH溶液等体积混合 |
| D.pH=2的CH3COOH和pH=12的NaOH溶液等体积混合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
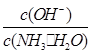 ________(填“增大”、“减小”或“不变”)。
________(填“增大”、“减小”或“不变”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH3·H2O(aq)十H+(aq) ΔH=bkJ·mol-1
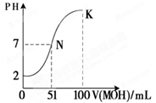
NH3·H2O(aq)十H+(aq) ΔH=bkJ·mol-1| A.随着盐酸的逐滴加入,水电离的c(OH—)总是逐渐减小 |
| B.当滴入10mL盐酸时,溶液中:c(NH4+)十c(NH3·H2O)=2c(Cl—) |
| C.当滴入20mL盐酸时,溶液中:c(Cl—)十c(H+)=c(NH4+)十c(OH—) |
D.水电离过程的热化学方程式可表示为:H2O(1)  H+(aq)+OH—(aq) ΔH=( b-a) kJ·mol-1 H+(aq)+OH—(aq) ΔH=( b-a) kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 =10-8,下列叙述正确的是
=10-8,下列叙述正确的是查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com