
分析 (1)碘不易溶于水,易溶于有机溶剂;
(2)水和植物油分层;
(3)食盐溶于水,水易挥发;
(4)酒精与甲苯互溶,但沸点不同;
(5)沙子不溶于水.
解答 解:(1)碘不易溶于水,易溶于有机溶剂,则利用萃取分离,故答案为:萃取;
(2)水和植物油分层,则利用分液分离,故答案为:分液;
(3)食盐溶于水,水易挥发,则利用蒸发除去食盐溶液中的水,故答案为:蒸发;
(4)酒精与甲苯互溶,但沸点不同,则利用蒸馏分离,故答案为:蒸馏;
(5)沙子不溶于水,则利用过滤分离饱和氯化钾溶液和沙子,故答案为:过滤.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L SO3中含有0.5NA个SO3分子 | |
| B. | 48g O3气体含有3NA个氧原子 | |
| C. | 在1L0.5mol•L-lFeCl3溶液中含有0.5NA个Fe3+ | |
| D. | 1.5 mol NO2与足量水反应,转移的电子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶 | B. | 试管 | C. | 分液漏斗 | D. | 250mL容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只被氧化 | B. | 被氧化与被还原的个数比为1:3 | ||
| C. | 只被还原 | D. | 氧化剂与还原剂的质量比是1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
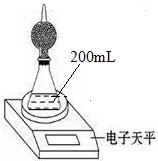 如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:| 实验操作 | t/min | 电子天平的读数/g |
| 装置+硫酸溶液 | 320.0 | |
| 装置+硫酸溶液+样品 | 0 | 335.0 |
| 1 | 334.5 | |
| 2 | 334.1 | |
| 3 | 333.8 | |
| 4 | 333.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com