


科目:高中化学 来源: 题型:
| A、向稀盐酸中加入少量钠粒:2Na+2H2O=2Na++2OH-+H2↑ |
| B、向氯化铁溶液中滴加偏铝酸钠溶液:Fe3++3AlO2-+6H2O=Fe(OH)3↓+3Al(OH)3↓ |
| C、Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++HCO3-+OH-=MgCO3↓+H2O |
| D、向含氯化铝的氯化镁溶液中加入氧化镁:Al3++MgO+H2O=Al(OH)3↓+Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下将0.1 mol?L-1 CH3COONa溶液与0.05 mol?L-1 HCl溶液等体积混合,c (Na+)>c (Cl-)>c(CH3COO-)>c (OH-)>c (H+) |
| B、常温下物质的量浓度相等的①NH4HSO4;②(NH4 )2CO3;③NH4Cl三种溶液中c(NH4+):①>③>② |
| C、常温下0.1mol?L-1的NaHA溶液,其pH=11,则溶液中:c(HA-)>c(OH-)>c(A2-)>c(H2A) |
D、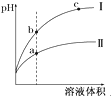 某温度下,相同pH的酸Ⅰ和酸Ⅱ溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断相同条件下酸性:Ⅰ>Ⅱ 某温度下,相同pH的酸Ⅰ和酸Ⅱ溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断相同条件下酸性:Ⅰ>Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
| B、1 L 0.1 mol?L-1 CuSO4?(NH4)2SO4?6H2O的溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| C、0.1 mol?L-1 NaHSO3溶液中:c(H+)+c(H2SO3)=c(SO32-)+c(OH-) |
| D、等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将Ca(ClO)2、Na2SO3、FeCl3溶液蒸干均得不到原溶质 |
| B、保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止Fe2+水解 |
| C、室温下,向0.1mol/L的CH3COOH溶液中加入少量水溶液显碱性的物质,CH3COOH的电离程度一定增大 |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com