
【题目】《茉莉花》是首脍炙人口的江苏民歌。乙酸苯甲酯可以从茉莉花中提取,也可用如图路线合成:
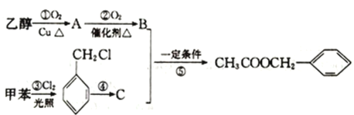
(1)乙酸苯甲酯的分子式为__,C的结构简式为__,B中所含官能团的名称为__,③的反应类型为___。
(2)①的化学方程式为___。
(3)乙酸苯甲酯与NaOH溶液反应的化学方程式为___。
【答案】C9H10O2 ![]() 羧基 取代反应 2CH3CH2OH+O2
羧基 取代反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O ![]() +NaOH
+NaOH![]() CH3COONa+
CH3COONa+![]()
【解析】
乙醇在Cu催化作用下加热反应生成A为CH3CHO,CH3CHO继续被氧化B为CH3COOH,乙酸和C发生酯化(取代)反应生成乙酸苯甲酯,则C是![]() ,甲苯和氯气在光照条件下发生取代反应生成一氯甲苯,一氯甲苯发生水解(取代)反应得C,结合有机物的结构和性质解答该题。
,甲苯和氯气在光照条件下发生取代反应生成一氯甲苯,一氯甲苯发生水解(取代)反应得C,结合有机物的结构和性质解答该题。
(1)根据乙酸苯甲酯结构简式知其分子式为C9H10O2,通过以上分析知,C为![]() ,B为CH3COOH,B中官能团是羧基,③为甲苯和氯气的取代反应,则该反应的反应类型为取代反应;
,B为CH3COOH,B中官能团是羧基,③为甲苯和氯气的取代反应,则该反应的反应类型为取代反应;
(2)①为乙醇的催化氧化反应生成乙醛和水,反应方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(3)乙酸苯甲酯中含有酯基,能碱性条件下能发生水解反应,反应方程式为![]() +NaOH
+NaOH![]() CH3COONa+
CH3COONa+![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室中有一未知浓度的稀盐酸,某学生为测定该盐酸的浓度在实验室中进行实验。请完成下列填空:
(1)配制100mL0.10mol/LNaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)__→洗涤(并将洗涤液移入容量瓶)→__→摇匀→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量__g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、___、__。
(2)取20.00mL待测盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下:
实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是___。
②根据上述数据,可计算出该盐酸的浓度约为__(保留两位有效数字)。
③排去碱式滴定管中气泡的方法应采用如图所示操作中的__,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:___。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F.碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mLNaOH溶液中投入10.8g的铝,二者恰好完全反应,试计算:
(1)求铝的物质的量___;
(2)参加反应的氢氧化钠的物质的量___和物质的量浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:![]() 时,
时,![]() ;
;![]() ;
;![]() 稀溶液中,
稀溶液中,![]() ;
;![]() ;
;![]() 红磷的化学式为P,白磷的化学式为
红磷的化学式为P,白磷的化学式为![]() ,已知:
,已知:
![]() ;
;![]()
![]() ;
;![]()
下列结论正确的是
A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低
B.稀硫酸和稀氢氧化钠溶液反应的中和热![]()
C.碳的燃烧热大于![]()
D.稀醋酸和稀氢氧化钠溶液反应生成1mol水,放出![]() 热量
热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。钴酸锂(LiCoO2)电池的工作原理如图所示,其中A极材料是金属锂和石墨的复合材料(石墨作金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许特定的离子通过。电池反应式为: LixC6+ Li1-xCoO2![]() C6+LiCoO2。下列说法中正确的是
C6+LiCoO2。下列说法中正确的是
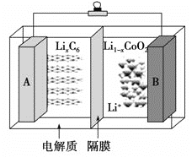
A.充电时Li由B极区域移向A极区域
B.充电时,A为阴极,发生氧化反应C6+xLi++xe-=LixC6
C.放电时,B为正极,电极反应式为Li1-xCoO2+xLi++xe-=LiCoO2
D.废旧钴酸锂(LiCoO2)电池进行“放电处理”使锂进入石墨中而有利于回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究氮氧化物的反应机理,对于消除其对环境的污染有重要意义。请回答下列与氮元素有关的问题:
(1)亚硝酸氯(结构式为Cl-N=O)是有机合成中的重要试剂。它可由Cl2和NO在通常条件下反应制得,反应方程式为2NO(g)+Cl2(g) ![]() 2ClNO(g)。已知几种化学的键能数据如下表所示:
2ClNO(g)。已知几种化学的键能数据如下表所示:

当Cl2与NO反应生成ClNO的过程中转移了4mol电子,理论上放出的热量为____kJ.
(2)在一个恒容密闭容器中充入2molNO(g)和1 mol Cl2(g)发生(1)中反应,在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间的关系如下表所示
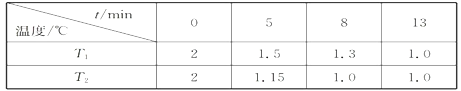
①T1________T2(填“>“”<”或”=”)。
②温度为T2℃时,在相同容器中,充入4molNO(g)和2mo1Cl2(g),则NO的平衡转化率___________50%(填“大于”、“等于”或“小于”)
③温度为T2℃时,起始时容器内的强为p0,则该反应的平衡常数Kp=______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-),其工作原理如图所示
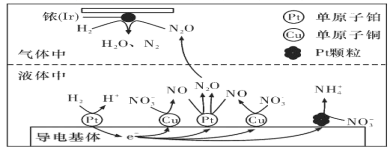
①Ir表面发生反应的方程式为_________________________________________________。
②若导电基体上的Pt颗粒增多,造成的后果是___________________________________。
II:利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示
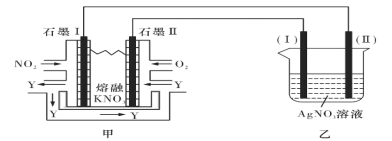
请回答下列问题:
(4)①甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨II负极发生的电极反应式为____________________________________________。
②若用10A的电流电解60min,已知该电解池的电解效率为80.4%,则乙中阴极得到____g质量的Ag。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为96500C/mol)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸亚铁可用于制备补血剂。某研究小组制备了FeCO3,并对FeCO3的性质和应用进行了探究。
已知:①FeCO3是白色固体,难溶于水
②Fe2++6SCN-![]() Fe(SCN)64-(无色)
Fe(SCN)64-(无色)
Ⅰ.FeCO3的制取(夹持装置略)
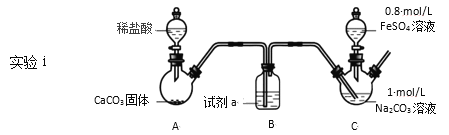
装置C中,向Na2CO3溶液(pH=11.9)通入一段时间CO2至其pH为7,滴加一定量FeSO4溶液,产生白色沉淀,过滤、洗涤、干燥,得到FeCO3固体。
(1)试剂a是__。
(2)向Na2CO3溶液通入CO2的目的是__。
(3)C装置中制取FeCO3的离子方程式为__。
(4)有同学认为C中出现白色沉淀之后应继续通CO2,你认为是否合理并说明理由__。
Ⅱ.FeCO3的性质探究
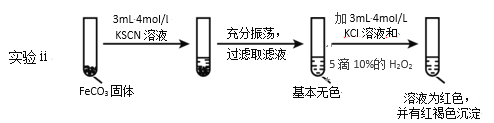
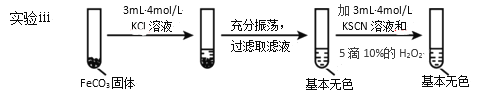
(5)对比实验ⅱ和ⅲ,得出的实验结论是__。
(6)依据实验ⅱ的现象,写出加入10%H2O2溶液的离子方程式__。
Ⅲ.FeCO3的应用
(7)FeCO3溶于乳酸[CH3CH(OH)COOH]能制得可溶性乳酸亚铁补血剂,此反应的离子方程式为__。该实验小组用KMnO4测定补血剂中亚铁含量进而计算乳酸亚铁的质量分数,发现乳酸亚铁的质量分数总是大于100%,其原因是__(不考虑操作不当引起的误差)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列物质:①氯气、②铜片、③碳酸钙、④蔗糖、⑤HCl气体、⑥SO2气体、⑦氨水,能导电的是________________,属于电解质的是_________________。(填编号)
(2)节日焰火利用的是____反应,城市射灯在夜空形成五颜六色的光柱,属于___效应。
(3)①除去铁粉中混用铝粉,选用的试剂为:___________;
②NaHCO3溶液中混有Na2CO3选用的试剂为_____________;
③除去Na2CO3粉末中的NaHCO3,采用的方法__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组研究NaOH与某些酸之间的反应。
Ⅰ.中和热的测定
在25℃、101kPa条件下,强酸与强碱的稀溶液中和热可表示为:H+(aq)+ OH─(aq)= H2O(l) △H =-57.3kJ·mol1。按照图所示装置进行实验。
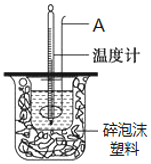
(1)仪器A的名称是______。
(2)碎泡沫塑料的作用是___________。
(3)在25℃、101kPa条件下,取50mL 0.50 mol·L1 CH3COOH溶液、50mL 0.55 mol·L1 NaOH溶液进行实验,测得的中和热△H____-57.3kJ·mol1(填“>”“=”或“<”)。
Ⅱ.中和滴定
(1)用酸式滴定管量取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加1~2滴酚酞作指示剂,用0.20 mol·L—1NaOH标准溶液进行滴定。为了减小实验误差,该同学一共进行了三次实验,假设每次所取稀盐酸体积均为20.00 mL,三次实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗NaOH溶液体积/mL | 19.00 | 23.00 | 23.02 |
该盐酸的浓度约为_________(保留两位有效数字)。滴定达到终点的标志是__________。
(2)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有_______。
A. 滴定终点读数时俯视读数
B. 酸式滴定管使用前,水洗后未用待测盐酸润洗
C. 锥形瓶水洗后未干燥
D. 配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中
E. 配制NaOH标准溶液时,定容时仰视容量瓶的刻度线
F. 碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com