
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | HCl |
分析 阴离子相同,阳离子不同,则加入NaOH溶液,NaCl无现象,NH4Cl有刺激性气体生成,AlCl3先生成白色沉淀,氢氧化钠过量,沉淀溶解,FeCl3生成红褐色沉淀,以此来解答.
解答 解:A.KSCN只能鉴别FeCl3,故A不选;
B.均不与氯化钡反应,不能鉴别,故B不选;
C.加入NaOH溶液,NaCl无现象,NH4Cl有刺激性气体生成,AlCl3先生成白色沉淀,氢氧化钠过量,沉淀溶解,FeCl3生成红褐色沉淀,现象不同可鉴别,故C选;
D.均与盐酸不反应,不能鉴别,故D不选;
故选C.
点评 本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质的异同,题目难度不大,鉴别时注意要有明显的现象.


科目:高中化学 来源: 题型:选择题
| A. | 含等物质的量的HCl、Na2CO3、CH3COOH的混合溶液 | |
| B. | 0.01mol•L-1的盐酸和pH=12的氢氧化钡溶液等体积混合 | |
| C. | 0.05mol•L-1的H2SO4溶液和0.1mol•L-1的KOH溶液等体积混合 | |
| D. | 非电解质溶于水得到的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,同浓度的一元酸HA比HB易电离,则相同浓度的NaA溶液比NaB溶液的pH大 | |
| B. | 0.2 mol/LNH4NO3 和 0.l mol/L NaOH 溶液等体积混合后:c(NH4+)>c (NO3-)>c (Na+)>c (OH-)>c (H+) | |
| C. | 物质的量浓度相等的醋酸溶液和氢氧化钠溶液等体积混合:c (Na+)+c(H+)=c (CH3COO-)+c (OH-)+c (CH3COOH) | |
| D. | 同浓度的下列溶液:①NH4Al(SO4)2②NH4Cl ③NH3•H2O ④CH3COONH4,其中c(NH4+) 由大到小的顺序是:①>②>④>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
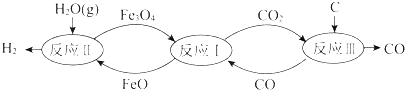
| A. | 反应Ⅰ的化学方程式是Fe3O4+CO?3FeO+CO2 | |
| B. | 反应Ⅱ的化学方程式是3FeO+H2O(g)?Fe3O4+H2 | |
| C. | 总反应的化学方程式是C+2H2O(g)?CO2+2H2 | |
| D. | 铁的氧化物是裂解水的催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在反应2 H2S+SO2→3 S+2 H2O中被氧化与被还原的硫原子的质量 | |
| B. | 相同温度下,0.2 mol•L-1 CH3COOH溶液与0.1 mol•L-1 CH3COOH溶液中的c(H+) | |
| C. | 在密闭容器中,N2+3H2?2NH3达平衡时的c(NH3)与c(N2) | |
| D. | Na2CO3晶体中Na+与CO32-离子个数比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5g CH3+含有的电子数为NA | |
| B. | 在lL 0.lmol/L氯化铝溶液中阳离子总数大于0.lNA | |
| C. | 标准状况下,11.2L四氯化碳中含有的C-CI键的个数为2NA | |
| D. | 60g SiO2和12g金刚石中各含有4NA个Si-O键和4NA个C-C键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
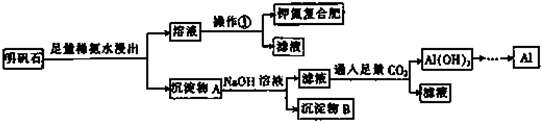
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾的化学式为:KAl(SO4)2 | |
| B. | 氯离子的结构示意图为: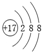 | |
| C. | 纯碱的化学式:NaCO3 | |
| D. | 氨水的电离方程式:NH3•H2O→NH4++H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com