
【题目】(1)微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示:
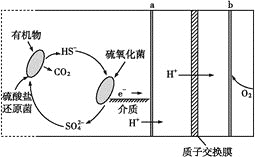
HS-在硫氧化菌作用下转化为SO![]() 的反应式是__。
的反应式是__。
(2)PbSO4热激活电池可用作火箭、导弹的工作电源,基本结构如图所示,其中作为电解质的无水LiCl—KCl受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。
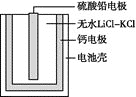
①放电过程中,Li+向__(填“负极”或“正极”)移动。
②负极反应式为__。
③电路中每转移0.2mol电子,理论上生成__gPb。
(3)氨氧燃料电池具有很大的发展潜力。氨氧燃料电池工作原理如图所示。
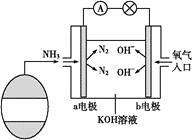
①a电极的电极反应式是__。
②一段时间后,需向装置中补充KOH,请依据反应原理解释原因:__。
【答案】HS-+4H2O-8e-=SO![]() +9H+ 正极 Ca+2Cl--2e-=CaCl2 20.7 2NH3-6e-+6OH-=N2+6H2O 由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH
+9H+ 正极 Ca+2Cl--2e-=CaCl2 20.7 2NH3-6e-+6OH-=N2+6H2O 由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH
【解析】
3个问题都是原电池相关的问题,应用原电池原理解本题即可,假如是燃料电池,通入燃料的电极是负极、通入氧化剂的电极为正极,还原剂在原电池的负极发生氧化反应,书写电极反应式时要结合电解质,(1)中有质子交换膜,由图知负极上有氢离子生成、正极上有氢离子反应,(2)是无水盐环境,(3)在碱性电解质溶液中,电极上不能生成H+,据此回答;
(1)由微生物燃料电池的图可知,HS-在硫氧化菌作用下转化为SO![]() 的同时,还产生了氢离子,根据质量守恒和电荷守恒可写出相关的反应式为
的同时,还产生了氢离子,根据质量守恒和电荷守恒可写出相关的反应式为![]() ;
;
故答案为:![]() ;
;
(2)①电池放电过程中,阳离子向正极移动,Li+向正极移动,
答案为:正极;
②由电池总反应式可知,负极上是钙放电,产物为氯化钙,据此可知负极反应式为:Ca+2Cl--2e-=CaCl2
答案为:Ca+2Cl--2e-=CaCl2;
③由反应中的化合价变化可知,每生成1molPb,转移电子数为2mol,故电路中每转移0.2mol电子,理论上生成0.1molPb,质量为0.1mol ×207g/mol=20.7g;
答案为:20.7;
(3)①由电池工作图可知,氨气在a电极放电,产生氮气,碱性条件下,还产生水,故a电极的电极反应式是2NH3-6e-+6OH-=N2+6H2O;
答案为:2NH3-6e-+6OH-=N2+6H2O;
②一段时间后,需向装置中补充KOH的原因是由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH;
故答案为:由于发生4NH3+3O2=2N2+6H2O反应,有水生成,使得溶液逐渐变稀,所以要补充KOH。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:
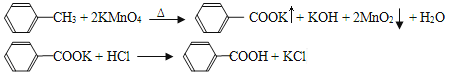
己知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。
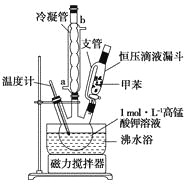
(1)图中冷凝管的进水口为________(填“a”或“b”)。支管的作用是___________。
(2)在本实验中,三领烧瓶最合适的容积___________(填字母)。
A.50mL | B.I00mL | C.200mL | D.250mL |
相对于用酒精灯直接加热,用沸水浴加热的优点是___________________。
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯
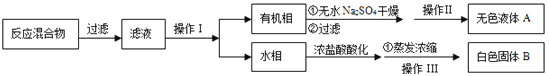
(3)操作Ⅰ的名称是 ;含有杂志的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是 。
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体加入水中,加热溶解,______。 | 得到白色晶体和无色溶液 | |
② | 取少重滤液于试管中,________。 | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________。 | _____________________ | 白色晶体是苯甲酸 |
纯度测定:称取1.220g产品,配成100ml甲醇溶液,取25.00ml溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
第一次 | 第二次 | 第三次 | 第四 | |
体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______________(填“偏大”、“偏小”或“不变”)。计算样品中苯甲酸纯度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图示代表周期表中的几种短周期元素,下列说法中错误的是()
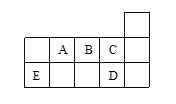
A. ED4分子中各原子均满足8电子稳定结构
B. AD3和ED4两分子的中心原子均为sp3杂化
C. C、D气态氢化物稳定性强弱为C>D
D. A、B、C电负性大小顺序为C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物(a)![]() 、(b)
、(b)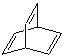 、(c)
、(c)![]() ,(d)
,(d)![]() ,下列说法不正确的是 ( )
,下列说法不正确的是 ( )
A. a、b、c、d互为同分异构体B. 除a外均可发生加成反应
C. c中所有原子不可能处于同一平面D. 一氯代物同分异构体最多的是c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下铁可以和 CO2 发生反应:Fe(s)+CO2(g)FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 CO2 气体,反应过程中 CO2 气体和 CO 气体的浓度与时间的关系如图所示:

(1)t1 时,正、逆反应速率的大小关系为 v 正_____v 逆(填“>”“<”或“=”)。
(2)4 min 内,CO 的平均反应速率 v(CO)=_____。
(3)下列条件的改变能减慢其反应速率的是_____(填序号,下同)。
①降低温度
②减少铁粉的质量
③保持压强不变,充入 He 使容器的体积增大
④保持容积不变,充入 He 使体系压强增大
(4)下列描述能说明上述反应已达平衡状态的是_____。
①v(CO2)=v(CO)
②单位时间内生成 n mol CO2 的同时生成 n mol CO
③容器中气体压强不随时间变化而变化
④容器中气体的平均相对分子质量不随时间变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扎来普隆是一种短期治疗失眠症的药物,其合成路线如下:

回答下列问题:
(1)A中的官能团名称是________________。
(2)![]() 所需的试剂和条件分别为________________。
所需的试剂和条件分别为________________。
(3)![]() 、
、![]() 的反应类型依次为________、________。
的反应类型依次为________、________。
(4)扎来普隆的分子式为________________。
(5)![]() 的化学方程式为________________________。
的化学方程式为________________________。
(6)属于芳香化合物,且含有硝基,并能发生银镜反应的B的同分异构体有________种(不考虑立体异构),其中核磁共振氢谱有4组峰的结构简式有________________。
(7)已知:![]() 有碱性且易被氧化。设计由
有碱性且易被氧化。设计由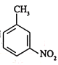 和乙醇制备
和乙醇制备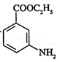 的合成路线(无机试剂任选)。________
的合成路线(无机试剂任选)。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年冬季,我国北方大部分地区出现严重雾霾天气,引起雾霾的PM2.5微细粒子包含(NH4)2SO4、NH4NO3、有机颗粒物及扬尘等。城市雾霾中还含有铜等重金属元素。
(1)N元素原子核外电子云的形状有___________种;基态铜原子的价电子排布式为___________,金属铜的晶体中,铜原子的堆积方式为___________。
(2)N和O中第一电离能较小的元素是___________;SO42-的空间构型___________。
(3)NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中心离子的配位数为___________。
(4)测定大气中PM2.5浓度的方法之一是β-射线吸收法,β-射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,晶胞边长为540pm,则该晶体的密度___________g/cm3(只列式不计算)(1pm=10-10cm)
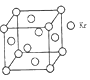
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫的催化氧化原理为2SO2(g)+O2(g)![]() 2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
2SO3(g)。在一定压强下,反应混合体系在平衡状态时SO3的百分含量与温度的关系如图所示。下列说法不正确的是
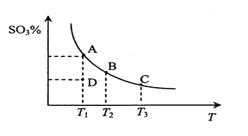
A. 反应2SO2(g)+O2(g)![]() 2SO3(g)的△H<0
2SO3(g)的△H<0
B. 在D点时v(正)<v(逆)
C. 若B、C点的平衡常数分别为KB、KC,则KB>KC
D. 恒温恒压下向平衡体系中通入氦气,平衡向左移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com