
| △c |
| △t |
| 0.30mol/L |
| 10min |
| (0.2+0.30+0.30)mol/L×10L |
| 5.0mol+4.5mol |
| c2(SO3) |
| c2(SO2)c(O2) |
| (0.3mol/L)2 |
| (0.2mol/L)2×0.3mol/L |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、核磁共振氢谱图上可以推知有机物分子中几种不同类型的氢原子及它们的数目 |
| B、红外光谱是用高能电子流等轰击样品分子,使分子失去电子变成分子离子或碎片离子 |
| C、质谱法具有慢速、微量、精确的特点 |
| D、紫外光谱可以确定有机物中的化学键和官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:
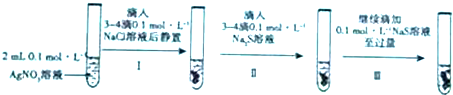
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 加入试剂 | 实验现象 |
| Ⅰ | 4mL 2mol/L NH4Cl 溶液 | 沉淀溶解 |
| Ⅱ | 4mL蒸馏水 | 沉淀不溶解 |
| 序号 | 实验内容 | 结 果 |
| 1 | 测定醋酸铵溶液的pH | pH约为7,溶液呈中性 |
| 2 | 取少量的相同质量的氢氧化镁分别盛放在试管中,分别向其中滴加醋酸铵溶液和氯化铵溶液 | 固体均溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化碳是主要的大气污染物 |
| B、聚二氧化碳塑料可以通过加聚反应制得 |
| C、CO2原子晶体具有较低的熔点和沸点 |
| D、CO2的原子晶体和聚二氧化碳塑料都属于纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
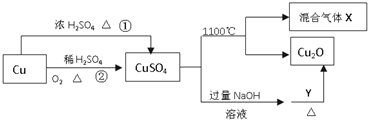
| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是蔗糖溶液 |
| C、CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D、将CuSO4溶液蒸发、冷却、结晶,可制得胆矾晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、发展循环经济,构建资源节约型社会及清洁生产技术 |
| B、采用绿色化学生产工艺,提高原子利用率,建立环境友好型化工体系 |
| C、大量砍伐森林,以满足人们对木材的需求 |
| D、大力开发可再生资源,推广用乙醇汽油代替传统的燃油 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com