
 ¶žŃõ»ÆĮņŗĶµŖµÄŃõ»ÆĪļŹĒ³£ÓĆµÄ»Æ¹¤ŌĮĻ£¬µ«Ņ²ŹĒ“óĘųµÄÖ÷ŅŖĪŪČ¾Īļ£®×ŪŗĻÖĪĄķĘäĪŪČ¾ŹĒ»·¾³»Æѧµ±Ē°µÄÖŲŅŖŃŠ¾æÄŚČŻÖ®Ņ»£®
¶žŃõ»ÆĮņŗĶµŖµÄŃõ»ÆĪļŹĒ³£ÓĆµÄ»Æ¹¤ŌĮĻ£¬µ«Ņ²ŹĒ“óĘųµÄÖ÷ŅŖĪŪČ¾Īļ£®×ŪŗĻÖĪĄķĘäĪŪČ¾ŹĒ»·¾³»Æѧµ±Ē°µÄÖŲŅŖŃŠ¾æÄŚČŻÖ®Ņ»£®·ÖĪö £Ø1£©øł¾ŻĶ¼±ķµĆ×Ŗ»ÆµÄSO2ĪŖ£ŗ2mol”Į0.80=1.6mol
2SO2£Øg£©+O2£Øg£©$\frac{\underline{“߻ƼĮ}}{”÷}$2SO3£Øg£©
n0 £Ømol£© 2.0 1.0 0
”÷n£Ømol£© 1.6 0.8 1.6
nĘ½£Ømol£© 0.4 0.2 1.6
¼ĘĖćĘ½ŗāŹ±ø÷ĪļÖŹµÄÅØ¶Č£¬æɼĘĖćĘ½ŗā³£Źż£»
£Ø2£©ČōøÄŌŚČŻĘ÷ÖŠ¼ÓČė1.0mol SO2”¢0.5mol O2ŗĶamol SO3£¬±£³ÖĪĀ¶Č²»±ä·“Ó¦“ļĘ½ŗāŗó£¬ĢåĻµ×ÜŃ¹ĒæŅ²ĪŖ0.10MPa£¬Ó¦ĪŖµČŠ§Ę½ŗā£»
£Ø3£©ĪĀ¶Č²»±ä£¬ŌņĘ½ŗā³£Źż²»±ä£®
½ā“š ½ā£ŗ£Ø1£©øł¾ŻĶ¼±ķµĆ×Ŗ»ÆµÄSO2ĪŖ£ŗ2mol”Į0.80=1.6mol
2SO2£Øg£©+O2£Øg£©$\frac{\underline{“߻ƼĮ}}{”÷}$2SO3£Øg£©
n0 £Ømol£© 2.0 1.0 0
”÷n£Ømol£© 1.6 0.8 1.6
nĘ½£Ømol£© 0.4 0.2 1.6
ČŻĘ÷Ģå»żĪŖ10LŌņø÷ĪļÖŹĘ½ŗāÅØ¶Č£ŗC£ØSO2£©=0.04mol/L C£ØO2£©=0.02mol/L C£ØSO3£©=0.16mol/L
K=$\frac{{c}^{2}£ØS{O}_{3}£©}{{c}^{2}£ØS{O}_{2}£©c£Ø{O}_{2}£©}$=$\frac{0.1{6}^{2}}{0.0{4}^{2}”Į0.02}$=800L/mol£¬
¹Ź“š°øĪŖ£ŗ800£»
£Ø2£©Į½“ĪĘ½ŗāĪŖµČŠ§Ę½ŗā£¬“ļµ½Ę½ŗāŗóø÷ĪļÖŹµÄĪļÖŹµÄĮæĻąĶ¬£®
2SO2£Øg£©+O2£Øg£© $\frac{\underline{“߻ƼĮ}}{”÷}$2SO3£Øg£©
n0 £Ømol£© 1.0 0.5 a
”÷n£Ømol£© 0.6 0.3 0.6
nĘ½£Ømol£© 0.4 0.2 1.6
a=1.0£¬
SO2Ę½ŗā×Ŗ»ÆĀŹ=$\frac{ĻūŗÄĮæ}{ĘšŹ¼Įæ}$”Į100%=$\frac{0.6}{1.0}$”Į100%=60%£¬
¹Ź“š°øĪŖ£ŗ1.0£»60%£»
£Ø3£©ÓÉÓŚĪĀ¶Č²»±ä£¬ŌņK²»±ä£¬Ę½ŗā³£ŹżK£ØA£©=K£ØB£©£¬¹Ź“š°øĪŖ£ŗ=£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆŃ§Ę½ŗāĶ¼Ļ󔢻ÆŃ§Ę½ŗā³£Źż”¢»ÆŃ§Ę½ŗāµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£¬ĢāÄæÉč¼ĘÖŖŹ¶µć¶ą£¬ÄѶČÖŠµČ£¬½āĢāŹ±×¢Ņāæ“ĒåĶ¼Ļ󣬰ŃĪÕČż¶ĪŹ½ŌŚĘ½ŗā¼ĘĖćµÄÓ¦ÓĆ£®


 ĢģĢģĻņÉĻæĪŹ±Ķ¬²½ŃµĮ·ĻµĮŠ“š°ø
ĢģĢģĻņÉĻæĪŹ±Ķ¬²½ŃµĮ·ĻµĮŠ“š°ø Ńō¹āæĪĢĆĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
Ńō¹āæĪĢĆĶ¬²½Į·Ļ°ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 æĘѧ¼ŅÕżŌŚŃŠ¾æĪĀŹŅĘųĢåCH4ŗĶCO2µÄ×Ŗ»ÆŗĶĄūÓĆ£®
æĘѧ¼ŅÕżŌŚŃŠ¾æĪĀŹŅĘųĢåCH4ŗĶCO2µÄ×Ŗ»ÆŗĶĄūÓĆ£®| ””””²ĪŹż ·Ö×Ó | ·Ö×ÓÖ±¾¶/nm | ·Ö×ÓÓėH2OµÄ ½įŗĻÄÜE/kJ•mol-1 |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
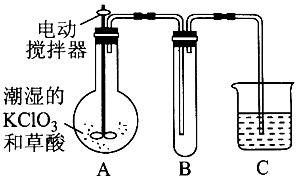
 ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅÖ®¼äµÄøō°åKŗĶ»īČūF¶¼æÉ×óÓŅŅĘ¶Æ£¬¼×ÖŠ³äČė2molAŗĶ1molB£¬ŅŅÖŠ³äČė2molCŗĶ1molHe£¬“ĖŹ±KĶ£ŌŚ0“¦£®ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśæÉÄę·“Ó¦£ŗ2A£Øg£©+B£Øg£©?2C£Øg£©£» ·“Ó¦“ļµ½Ę½ŗāŗó£¬ŌŁ»Öø“ÖĮŌĪĀ¶Č£®»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅÖ®¼äµÄøō°åKŗĶ»īČūF¶¼æÉ×óÓŅŅĘ¶Æ£¬¼×ÖŠ³äČė2molAŗĶ1molB£¬ŅŅÖŠ³äČė2molCŗĶ1molHe£¬“ĖŹ±KĶ£ŌŚ0“¦£®ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśæÉÄę·“Ó¦£ŗ2A£Øg£©+B£Øg£©?2C£Øg£©£» ·“Ó¦“ļµ½Ę½ŗāŗó£¬ŌŁ»Öø“ÖĮŌĪĀ¶Č£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ±ķÖŠŹµĻߏĒŌŖĖŲÖÜĘŚ±ķµÄ²æ·Ö±ß½ē£¬ĘäÖŠÉĻ±ß½ēĪ“ÓĆŹµĻß±ź³ö£®
±ķÖŠŹµĻߏĒŌŖĖŲÖÜĘŚ±ķµÄ²æ·Ö±ß½ē£¬ĘäÖŠÉĻ±ß½ēĪ“ÓĆŹµĻß±ź³ö£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £»
£»²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com