
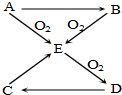
 ŅŃÖŖA”¢B”¢C”¢D”¢EĪåÖÖĪļÖŹÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£Ø²æ·Ö·“Ó¦Īļ¼°·“Ó¦Ģõ¼žĪ“ĮŠ³ö£¬Čō½āĢāŹ±ŠčŅŖ£¬æÉ×÷ŗĻĄķ¼ŁÉč£©£¬ĒŅĪåÖÖĪļÖŹÖŠ¾łŗ¬ÓŠAŌŖĖŲ£®
ŅŃÖŖA”¢B”¢C”¢D”¢EĪåÖÖĪļÖŹÓŠČēĶ¼ĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ£Ø²æ·Ö·“Ó¦Īļ¼°·“Ó¦Ģõ¼žĪ“ĮŠ³ö£¬Čō½āĢāŹ±ŠčŅŖ£¬æÉ×÷ŗĻĄķ¼ŁÉč£©£¬ĒŅĪåÖÖĪļÖŹÖŠ¾łŗ¬ÓŠAŌŖĖŲ£®·ÖĪö A”¢B”¢C”¢D”¢E¾łŗ¬ÓŠAŌŖĖŲ£¬AÓėŃõĘųæÉŅŌĮ¬Šų·“Ó¦µĆµ½D£¬A×Ŗ»ÆµĆµ½B£¬¶ųBÓėŃõĘų·“Ó¦æÉŅŌµĆµ½E£¬ĖµĆ÷AÖŠµÄŌŖĖŲŹĒ±ä¼ŪŌŖĖŲ£®
£Ø1£©ČōAĪŖĘųĢåµ„ÖŹ£¬ĶʶĻAĪŖN2£¬ŌņBĪŖNH3£¬EĪŖNO£¬DĪŖNO2£¬CĪŖHNO3£»
£Ø2£©ČōAĪŖ¹ĢĢåµ„ÖŹ£¬ĒŅŅ×ČÜÓŚ¶žĮņ»ÆĢ¼£¬ŌņAĪŖS£¬æÉÖŖBĪŖH2S£¬EĪŖSO2£¬DĪŖSO3£¬CĪŖH2SO4£®
½ā“š ½ā£ŗA”¢B”¢C”¢D”¢E¾łŗ¬ÓŠAŌŖĖŲ£¬AÓėŃõĘųæÉŅŌĮ¬Šų·“Ó¦µĆµ½D£¬A×Ŗ»ÆµĆµ½B£¬¶ųBÓėŃõĘų·“Ó¦æÉŅŌµĆµ½E£¬ĖµĆ÷AÖŠµÄŌŖĖŲŹĒ±ä¼ŪŌŖĖŲ£®
£Ø1£©ČōAĪŖĘųĢåµ„ÖŹ£¬ĶʶĻAĪŖN2£¬ŌņBĪŖNH3£¬EĪŖNO£¬DĪŖNO2£¬CĪŖHNO3£®
¢ŁB”śEµÄ»Æѧ·½³ĢŹ½£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£¬
¹Ź“š°øĪŖ£ŗ4NH3+5O2$\frac{\underline{“߻ƼĮ}}{”÷}$4NO+6H2O£»
¢Ś·¢Éś·“Ó¦£ŗ3NO2+H2O=2HNO3+NO£¬3Ģå»ż¶žŃõ»ÆµŖ·“Ӧɜ³É1Ģå»żNO£¬ČÜŅŗĢå»żĪŖ2Ģå»ż£¬Įī¶žŃõ»ÆµŖĪŖ3mol£¬ŌņÉś³ÉĻõĖįĪŖ2mol£¬ČÜŅŗĢå»żĪŖ2L”Į22.4L/mol£¬Ōņ×īÖÕÉÕĘæÄŚĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ$\frac{2mol}{2mol”Į22.4L/mol}$=0.045mol/L£¬
¹Ź“š°øĪŖ£ŗ0.045 mol/L£»
£Ø2£©ČōAĪŖ¹ĢĢåµ„ÖŹ£¬ĒŅŅ×ČÜÓŚ¶žĮņ»ÆĢ¼£¬ŌņAĪŖS£¬æÉÖŖBĪŖH2S£¬EĪŖSO2£¬DĪŖSO3£¬CĪŖH2SO4£®
¢ŁDµÄ·Ö×ÓŹ½ĪŖ£ŗSO3£¬¹Ź“š°øĪŖ£ŗSO3£»
¢ŚC”śEµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCu+2H2SO4£ØÅØ£© CuSO4+SO2”ü+2H2OµČ£¬
¹Ź“š°øĪŖ£ŗCu+2H2SO4£ØÅØ£© CuSO4+SO2”ü+2H2O£»
¢Ū½«EĶØČėijŠ©µ„ÖŹµÄČÜŅŗÖŠ£¬æÉ·¢Éś·“Ӧɜ³ÉĮ½ÖÖĒæĖį£¬ŹŌ¾ŁŅ»ĄżŠ“³ö»Æѧ·½³ĢŹ½ĪŖ£ŗSO2+Cl2+2H2O=2HCl+H2SO4£¬
¹Ź“š°øĪŖ£ŗSO2+Cl2+2H2O=2HCl+H2SO4£®
µćĘĄ ±¾Ģāæ¼²éĮĖĪŽ»śĪļÖŹµÄĶʶĻ£¬»ł±¾ŹōÓŚæŖ·ÅŠŌĢāÄ棬²ąÖŲæ¼²éĮņ”¢µŖŌŖĖŲµ„ÖŹ¼°Ęä»ÆŗĻĪļŠŌÖŹ£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļŠŌÖŹ£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 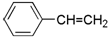 | B£® | 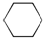 | C£® | 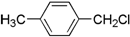 | D£® | 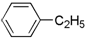 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
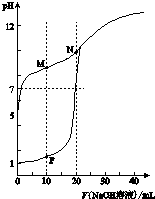 ÓĆ0.1mol•L-1 NaOHČÜŅŗ·Ö±šµĪ¶ØĢå»ż¾łĪŖ20mL”¢ÅØ¶Č¾łĪŖ0.1mol•L-1 HClČÜŅŗŗĶHXČÜŅŗ£¬ČÜŅŗµÄpHĖę¼ÓČėNaOHČÜŅŗĢå»ż±ä»ÆČēĶ¼£ŗ
ÓĆ0.1mol•L-1 NaOHČÜŅŗ·Ö±šµĪ¶ØĢå»ż¾łĪŖ20mL”¢ÅØ¶Č¾łĪŖ0.1mol•L-1 HClČÜŅŗŗĶHXČÜŅŗ£¬ČÜŅŗµÄpHĖę¼ÓČėNaOHČÜŅŗĢå»ż±ä»ÆČēĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2+2H2OØT2Na++2OH-+H2”ü | B£® | 2O22-+4H+ØT4OH-+O2”ü | ||
| C£® | Na2O2+2H2OØT2Na++2OH-+O2”ü | D£® | 2Na2O2+2H2OØT4Na++4OH-+O2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
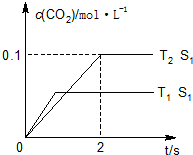 Ęū³µĪ²Ęų”¢Č¼ĆŗĪ²Ęų”¢µŲĆę»Ņ³¾µČĪŪČ¾ĪļŹĒŌģ³ÉæÕĘųĪŪČ¾µÄÖ÷ŅŖŌŅņ£®
Ęū³µĪ²Ęų”¢Č¼ĆŗĪ²Ęų”¢µŲĆę»Ņ³¾µČĪŪČ¾ĪļŹĒŌģ³ÉæÕĘųĪŪČ¾µÄÖ÷ŅŖŌŅņ£®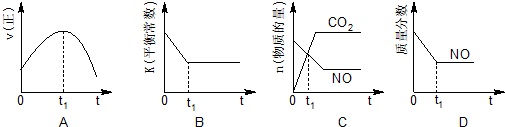
| ŹµŃé×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗā ĖłŠčŹ±¼ä/min | ||
| CO2£Øg£© | H2£Øg£© | H2O£Øg£© | CO2£Øg£© | |||
| 1 | 650 | 2 | 1 | 0.4 | 1.6 | 6 |
| 2 | 900 | 4 | 2 | 1.6 | 2.4 | 2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŅĻ©”¢ŅŅČ² | B£® | 1-¼ŗĻ©”¢¼×±½ | C£® | ±½”¢Õż¼ŗĶé | D£® | ±ūĶé ±ūČ² |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Š”ĖÕ“ņNaHCO3 | B£® | ÉÕ¼īNaOH | C£® | ĀĢ·ÆFeSO4•7H2O | D£® | ±µ²ĶBaCO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ćæ×ŖŅĘ0.1molµē×Ó£¬ĄķĀŪÉĻÉś³É20.7g Pb | |
| B£® | ³£ĪĀŹ±£¬ŌŚÕżøŗ¼«¼ä½ÓÉĻµēĮ÷±ķ»ņ¼ģĮ÷¼Ę£¬ÖøÕė²»Ę«×Ŗ | |
| C£® | Õż¼«·“Ó¦Ź½£ŗPb2++2e-ØTPb | |
| D£® | ·Åµē¹ż³ĢÖŠ£¬Li+Ļņøŗ¼«ŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com