
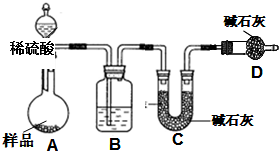
|
| 0.15mol��84g/mol |
| 17.90g |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4+ |
| B��NO2 |
| C��NO |
| D��N2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 MԪ�صĵ��ʿ�����ԭ�ӷ�Ӧ�ѵĵ��ȼ�����ԭ�ӽṹʾ��ͼ��ͼ��ʾ����
MԪ�صĵ��ʿ�����ԭ�ӷ�Ӧ�ѵĵ��ȼ�����ԭ�ӽṹʾ��ͼ��ͼ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� ���� | IA | 0 | ||||||
| 1 | �� | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | �� | �� | �� | |||||
| 3 | �� | �� | �� | �� | �� | |||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѹǿ��atm�� | 4 | 6 | 10 | 20 |
| D��Ũ�ȣ�mol?L-1�� | 0.085 | 0.126 | 0.200 | 0.440 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
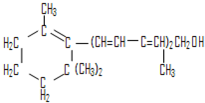 ά����A�������ر��Ƕ��˵���������Ҫ���ã���ṹ��ʽ��ͼ��
ά����A�������ر��Ƕ��˵���������Ҫ���ã���ṹ��ʽ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����λʱ������n mol��A2ͬʱ����n mol��AB |
| B�������ڵ���ѹǿ����ʱ��仯 |
| C�������ڵ������ܶȲ���ʱ��仯 |
| D����λʱ��������n mol��A2ͬʱ����n mol��B2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com