
【题目】在1273 K时,有如下反应:FeO(s) + CO(g) ![]() Fe(s) + CO2(g) K = 0.5
Fe(s) + CO2(g) K = 0.5
(1)、请写出求此反应平衡常数K的数学表达式:K=_____________________。
(2)、如果CO和CO2的起始浓度为下列数值:c (CO) = 0.05 mol·L--1 ,c (CO2) = 0.01 mol·L--1 ,求它们的平衡浓度_________。(写出计算过程)
(3)、平衡时,求CO的转化率为________________(不用写计算过程)。
【答案】 ![]() 解:设CO的转化浓度为x
解:设CO的转化浓度为x
FeO(s) + CO(g) ![]() Fe(s) + CO2(g)
Fe(s) + CO2(g)
c0/mol·L--1 0.05 0.01
Δc/ mol·L--1 x x
c(平)/ mol·L--1 0.05 -- x 0.01 + x
![]() 解得:x = 0.01 mol·L--1
解得:x = 0.01 mol·L--1
则c (CO) = 0.05 mol·L--1 -- 0.01 mol·L--1 = 0.04 mol·L--1
c (CO2) = 0.01 mol·L--1 + 0.01 mol·L--1 = 0.02 mol·L--1 20%
【解析】本题主要考查关于平衡常数的计算。
(1)此反应平衡常数K的数学表达式:K=![]() 。
。
(2)设CO的转化浓度为xmol·L-1,则CO和CO2的平衡浓度为:c(CO)=(0.05-x)mol·L-1,c(CO2)=(0.01+x)mol·L-1, ![]() ,解得:x=0.01。
,解得:x=0.01。
CO和CO2的平衡浓度为:c(CO)=(0.05-x)mol·L--1,=0.04 mol·L-1,c(CO2)=(0.01+x)mol·L--1=0.02mol·L-1。
(3)平衡时,CO的转化率为x/0.05=20%。


科目:高中化学 来源: 题型:
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜:3CuO+2NH3 ![]() 3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应.
3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应. 
(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是: .
(2)B中加入的是碱石灰,其作用是 .
(3)D中收集到的物质是 , 检验该物质的方法现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电子工业常用一定浓度的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板。现将一块敷有铜箔的绝缘板没入500mL某浓度FeCl3溶液中,一段时间后,将该线路板取出,向所得溶液中加入一定量的铁粉,充分反应后有固体剩余;将固体滤出并从滤液中取出20.00mL,向其中滴入2.00mol/LAgNO3溶液60.00 mL时,溶液中的Cl-恰好完全沉淀。请回答下列有关问题(忽略反应前后溶液体积的变化):
(1)原FeCl3溶液的物质的量浓度为_____________________。
(2)假若剩余固体中有铁粉,则向溶液中加入的铁粉质量至少应当大于_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间的转化都能通过一步实现的是( )
A. Si→SiO2→H2SiO3→Na2SiO3 B. Al→Al2O3→NaAlO2→Al(OH)3
C. S→SO3→H2SO4→SO2 D. N2→NO2→HNO3→NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是医药上常用的一种药剂,合成路线如图所示。其中A是相对分子质量为58的链状烃,其核磁共振氢谱上的峰面积之比为9:1,G为五元环状有机化合物。
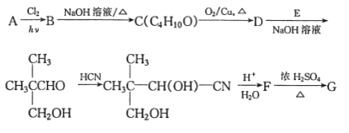
已知:①R'-CH2-CHO+RCH2-CHO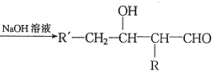
②RCN在酸性条件下水解变成RCOOH
(1)D分子中含有的官能团名称是___________。
(2)B→D反应过程中涉及的反应类型有_______________。
(3)A的结构简式为___________;E的结构简式为______________。
(4)F→G的化学方程式为____________。F能发生缩聚反应,则生成链节的主链上有四个碳愿子的高分子化合物的结构简式为_____________。
(5)同时满足下列条件G的同分异构体有_______种。(不包括立体异构)
①能发生银镜反应; ②能与NaHCO3发生反应。
其中核磁共振氢谱为4组峰的结构简式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重ag,另一电极上产生标准状况下的气体VmL。下列说法正确的是

A. 铜电极连接电源正极 B. 铜的相对原子质量的计算式是![]()
C. 黑色粉末X是铁粉 D. 石墨电极上发生的反应是4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O ![]() H++OH-;ΔH > 0,下列叙述正确的是( )
H++OH-;ΔH > 0,下列叙述正确的是( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中通入HCI气体,pH值减小,KW不变
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)增大
D. 将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/ mol·l-1 | 0.010 | 0.020 | 0.020 |
C(CO2)/ mol·l-1 | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A. 平衡时,乙中CO2 的转化率大于60%
B. 平衡时,甲和丙中H2 的转化率均是60%
C. 平衡时,丙中C(CO2)是甲中的2倍,是0.012 mol·l-1
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com