
��һ����ɱ���ܱ������У�����һ������X��Y��������ӦmX��g�� nY��g�� ��H��Q kJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������������ݻ����Ĺ�ϵ���±���ʾ��
nY��g�� ��H��Q kJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������������ݻ����Ĺ�ϵ���±���ʾ��
�������/L c ��Y��/mol��L��1 �¶�/�� | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1. | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
����˵����ȷ����
A��m>n
B��Q<0
C���¶Ȳ��䣬ѹǿ����Y��������������
D��������䣬�¶����ߣ�ƽ�����淴Ӧ�����ƶ�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����д��ȷ���ǣ� ��
A��ˮ������ͨ�������������Na2SiO3+SO2+H2O�T2Na++SO32��+H2SiO3��
B����м���ڹ���ϡ���3Fe+8H++2NO3-=3Fe2++2NO��+4H2O
C����̼����еμ�ϡ���CO32-+2H+=H2O+CO2��
D����NaOH��Һ�м�������Ca(HCO3)2��Һ��Ca2++2HCO3-+2OH-=CaCO3��+CO32-+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ�����и�һ10���¿���ѧ���������棩 ���ͣ�ѡ����
���з�Ӧ������������ԭ��Ӧ����ˮ�Ȳ����������ֲ�����ԭ�����ǣ� ��
A. SO3+H2O H2SO4 B. 3NO2+H2O
H2SO4 B. 3NO2+H2O 2HNO3+NO
2HNO3+NO
C. 2F2+2H2O 4HF+O
4HF+O 2 D. 2Na+2H2O
2 D. 2Na+2H2O 2NaOH+H2��
2NaOH+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶�10���¿���ѧ���������棩 ���ͣ�ʵ����
ij��ѧ��ȤС����һ��ʵ��̽���з��֣��������Һ����μ������Ը��������Һʱ����Һ��ɫ������죬����Ӧ������С���С���ԱΪ�ˡ��쳣������չ�����ۣ����������������������ԭ�������֣���Ϊ�����ʵ�����̽����֤��
����˷�Ӧ���̷��ȣ��¶����ߣ���Ӧ���ʼӿ죻
���������
��ʵ��Ŀ�ġ�̽�������������ط�Ӧ�����ʱ仯���쳣��ԭ��
��ʵ����Ʒ���������Թܡ���ͷ�ιܡ���Ͳ��ҩ�ס��������ȣ�
�Լ���0.1mol/L H2C2O4��Һ��0.05mol/L KMnO4�������ữ����Һ�ȡ�
������ݸ���ȤС���ʵ��̽�����˼·������������ȱ���ݡ�
��1�����ᣨH2C2O4�����ᣩ������KMnO4��Һ��Ӧ�����ӷ���ʽΪ
��2��Ҫ��ɶԲ�����ʵ����֤�����ٻ���Ҫһ��ʵ��������
��3����������:___________________
Ҫ���ʵ����֤������и�ʵ�黹Ҫ����һ���Լ���һ���������ֱ���
��4�����ڲ�����������Ʒ�������ʵ�飬���������ʵ���¼�����ݡ�
�Թ�A | �Թ�B | |
�����Լ� | ||
ʵ��������ɫʱ�䣩 | ||
���� | �������ȷ | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶�10���¿���ѧ���������棩 ���ͣ�ѡ����
ȡ��ȷ�NO2 ���ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У��������·�Ӧ��2NO2��g�� 
 N2O4��g�� ��H��0����Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO2�İٷֺ�����NO2%�������������淴Ӧ�¶ȣ�T���仯�Ĺ�ϵͼ������ʾ��ͼ�У�������ʵ�����������
N2O4��g�� ��H��0����Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO2�İٷֺ�����NO2%�������������淴Ӧ�¶ȣ�T���仯�Ĺ�ϵͼ������ʾ��ͼ�У�������ʵ�����������
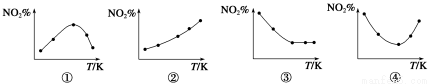
A���٢� B���٢� C���ڢ� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶�10���¿���ѧ���������棩 ���ͣ�ѡ����
����������100 mL 0.01 mol/L��ϡ���ᣨ��������Ӧ����Ӧ����̫����Ϊ�˼ӿ�˷�Ӧ���ʶ����ı�H2����������ʹ�����·����е�: �ټ�H2O �ڼ�NaOH���� �۵��뼸��Ũ���� �ܼ�CH3COONa���� �ݼ�NaCl��Һ ���뼸������ͭ��Һ �������¶ȣ�����������ӷ��� �����10 mL 0.1 mol/L��������100mL0.1 mol/L��ϡ����
A���٢ޢ� B���ۢݢ�� C���ۢߢ� D���ۢߢ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶�10���¿���ѧ���������棩 ���ͣ�ѡ����
�£�N2H4����һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯����ͼ��ʾ����֪����1mol��ѧ�������������kJ����N��NΪ942��O��OΪ500��N��NΪ154�������1molN��H�������������kJ���ǣ� ��
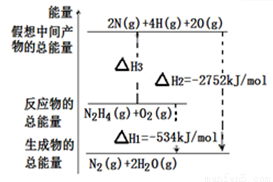
A��194 B��391 C��516 D��658
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ɹŸ߶������л�ѧ���������棩 ���ͣ�ѡ����
�������������ѧԭ�ϵ��м��壬��ṹ��ͼ�����й��ڿ������˵���в� ��ȷ���ǣ� ��
��ȷ���ǣ� ��
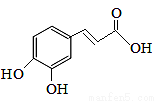
A���ܷ����Ӿ۷�Ӧ
B������̼������Һ��Ӧ
C��1 mol�������������3 mol NaOH��Ӧ
D��1 mol������������� 3 mol Br2��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ʵ����
���������£��赥�ʺ�HCl��Ӧ����SiHCl3�Ǵֹ��ᴿ����Ҫ���衣ijС�������ͼ��ʾװ���������ת�����г�װ����ȥ����
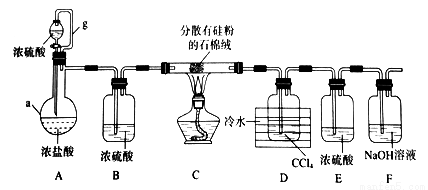
��֪��SiHCl3�ķе�Ϊ33.0��C���������л��ܼ�������ˮ���ҷ�Ӧ���ڿ������ױ�������CCl4�ķе�Ϊ76.8��C����ش�
��1������a������Ϊ ������g������Ϊ ��
��2��װ��A�У�Ũ�������ֵ�����Ϊ  ��ʵ��ʱ�����ȴ�Һ©��������һ��ʱ����ڵ�ȼC���ƾ��ƣ������� ��
��ʵ��ʱ�����ȴ�Һ©��������һ��ʱ����ڵ�ȼC���ƾ��ƣ������� ��
��3��װ��C�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��4��װ��D�����õ�Һ̬�����ķ��뷽��Ϊ ������������ƣ�
��5����Ӧ�������ͨ��װ��F�е�NaOH��Һ���ݳ�����Ĵ�������Ϊ ��
��6��SiHCl3�ڳ�ʪ�Ŀ����б�����������һ���������һ�������ᣬ�÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com