W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ
14��������Ϊ7��X��������NH
4+������ͬ�����ӡ�������Ŀ��W��Y����������ܵ���������γɣ�Z�ķǽ�������ͬ��������Ԫ������ǿ��

��1��Y�����ڱ��е�λ����
��
��2������һ��������NH
4+������ͬ�����ӡ�������Ŀ�������ӵĻ�ѧʽΪ
��
��3��X
3W��ˮ���ͷų�ʹ��̪��Һ��������A����ѧ����ʽ��
��
��4���ö��Ե缫��⻯����XZ��Һ�������ͷų�����B����Ӧ�����ӷ���ʽ��
��
��5����֪W�ĵ���������B��һ�������¿��γ�����A������
W
2��g��+3B��g��?2A��g����H=-92.4kJ?mol
-1��ij�¶�ʱ��һ���ݻ��̶����ܱ������У�����������Ӧ���ڲ�ͬʱ��ⶨ�������ڸ����ʵ�Ũ�����±���
| ʱ�� |
Ũ�ȣ�mol/L�� |
| c��W2�� |
c��B�� |
c��A�� |
| ��0min |
4.0 |
9.0 |
0 |
| ��10min |
3.8 |
8.4 |
0.4 |
| ��20min |
3.4 |
7.2 |
1.2 |
| ��30min |
3.4 |
7.2 |
1.2 |
| ��40min |
3.6 |
7.8 |
0.8 |
��W
2��ƽ����Ӧ����
| v(0min-10min) |
| v(10min-20min) |
=
��
�ڷ�Ӧ�ڵ�10min�ı��˷�Ӧ�������ı������������
��
a�������˴��� b�������¶� c������ѹǿ d������B��Ũ��
������Ӧ�ӵ�30minĩ�ַ�����һ�������ı䣬�ı�ķ�Ӧ����������
�����ݻ�ѧ��Ӧԭ����������������W
2ת���ʵ�Ӱ��
��




 ����ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D��E�������ʣ�
����ͨ����ͬ��ѧ��Ӧ�ֱ��Ƶ�B��C��D��E�������ʣ�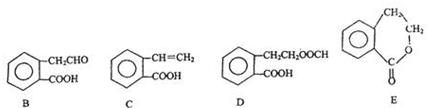
 ��HCOOH��CH3COOC2H5
��HCOOH��CH3COOC2H5
