
在容积不变的密闭容器中反应:N2+3H22NH3达到平衡,若将平衡体系中各物质的浓度都增大到原来的2倍,则产生的结果是( )
A.平衡向正反应方向移动
B.平衡不移动
C.平衡向逆反应方向移动
D.正反应速率增大,逆反应速率减小
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
下图中四条曲线分别表示ⅣA、ⅤA、ⅥA、ⅦA族元素的气态氢化物的沸点,a、b、c分别为三种氢化物,

(1)其中表示ⅥA元素气态氢化物沸点的是曲线________(填标号,下一空同),表示ⅣA族元素气态氢化物沸点的是曲线________。
(2)a的电子式为________,b的空间构型为________,c的化学式为________。
(3)同一族中第3、4、5周期元素的气态氢化物沸点依次升高,其原因是________________。曲线中第2周期元素的气态氢化物的沸点显著高于第3周期元素气态氢化物的沸点,其原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )

A.原子半径Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第2周期、第ⅥA族
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,将1mol的CO和水蒸气通入容器中发生下述反应:CO(g)+H2O(g)CO2(g)+H2(g),达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,又达到平衡后,CO2的物质的量是( )
A.等于0.6mol
B.等于1mol
C.大于0.6mol小于1mol
D.大于1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中充入3mol气体A和2.5mol气体B,发生反应:3A(g)+B(g)xC(g)+2D(g)(正反应为吸热反应),5min时测得生成1mol D,C的平均反应速率v(C)=0.1mol·L-1·min-1,试求:
(1)方程式中C的化学计量数x=__________。
(2)5min内A的平均反应速率v(A)=__________。
(3)5min时B的转化率为__________。
(4)温度升高A的转化率________(填“增大”或“减小”或“不变”下同),压强增大B的转化率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下的密闭容器中,进行如下反应:NO(g)+CO(g)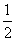 N2(g)+CO2(g) ΔH=-373.2 kJ·mol-1,为提高该反应的反应速率,缩短达到平衡的时间,下列措施不正确的是( )
N2(g)+CO2(g) ΔH=-373.2 kJ·mol-1,为提高该反应的反应速率,缩短达到平衡的时间,下列措施不正确的是( )
A.加(正)催化剂
B.增大压强(体积减小)
C.给体系加热
D.从体系中不断移去部分CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
在某温度下,将H2和I2各0.10 mol的气态混合物充入10 L的密闭容器中,充分反应,达到平衡后,测得=0.0080 mol·L-1。
(1)求该反应的平衡常数。
(2)在上述温度下,该容器中若通入H2和I2蒸气各0.20 mol,试求达到化学平衡状态时各物质的浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
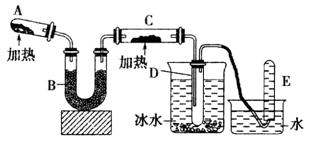
回答下列问题:
(1)A中生成氨气反应的化学方程式是_________________________________________;
(2)B中加入的干燥剂是_________(填序号)①浓硫酸②无水氯化钙 ③碱石灰;
(3)能证明氨与氧化铜反应的现象①C中______________、②D中有无色液体生成;
设计实验检验D中无色液的成分:取少量液体于试管中,加入少量________粉末,现象为___________________。
(4)写出氨气与氧化铜反应的化学方程式___________________________;若收集到2.24L(STP)氮气,计算转移电子数为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用石墨作电极电解下列溶液①稀H2SO4②K2SO4溶液 ③CuCl2溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1的是(填序号)____________
______,其阳极的电极反应式都是____________________________________________,
阴极的电极反应式都是_______________________________________________,
总反应的化学方程式都是_____________________________________________。
(2)阴极、阳极都有气体产生,其中溶液pH变小的是____,pH变大的是______。(填序号)
(3)一个电极析出金属,一个电极逸出气体,且溶液pH明显减小的是____________(填序号),其总反应的化学方程式是____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com