
| A. | 玻璃制品 | B. | 石英钟表 | C. | 计算机芯片 | D. | 光导纤维 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.4g | B. | 3.6g | C. | 4.8g | D. | 6.0g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②③⑥ | C. | ①⑥ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
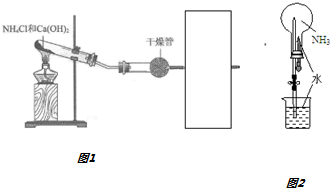
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA | |
| D. | 5.6gFe与0.1mol Cl2完全反应,反应中转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+才检验:加入NaOH浓溶液,加热,将润湿的蓝色石蕊试纸放在试管口 | |
| B. | Cl-检验:加入稀硝醉酸化,再加AgNO3溶液 | |
| C. | SO42-检验:加入稀盐酸酸化,再加BaCl2溶液 | |
| D. | K+检验:进行焰色反应,透过蓝色钻玻璃观察 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中K+、Ca2+、ClO-、Br-可以大量共存 | |
| B. | 能使含I2的淀粉溶液蓝色褪去,说明NaHSO3溶液具漂白性 | |
| C. | NaHSO3溶液c(Na+)+c(H+)=c(HSO3-)+c(SO32-)+c(OH-) | |
| D. | 和足量Ca(OH)2溶液反应的离子方程式:Ca2++OH-+HSO3-=CaSO3↓+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com