
【题目】关于第三周期元素性质的说法正确的是( )
A. 镁单质能和冷水发生剧烈的反应 B. 碱性Mg(OH)2<Al(OH)3
C. 稳定性SiH4<HCl D. 金属性Na<Mg
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.蚕丝、羊毛、棉花的成分都是蛋白质
B.蛋白质溶液不能产生丁达尔效应
C.向蛋白质溶液中加入CuSO4溶液,产生盐析现象
D.蛋白质在紫外线的照射下将会失去生理活性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较不同的催化剂对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验.下列叙述中不正确的是( ) 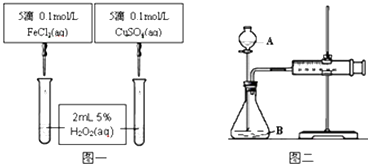
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置可测定反应产生的气体体积
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)═2CO2(g)△H=﹣566kJmol﹣1
N2(g)+O2(g)═2NO(g)△H=+180kJmol﹣1
则2CO(g)+2NO(g)═N2(g)+2CO2(g)的△H是( )
A.﹣386 kJmol﹣1
B.+386 kJmol﹣1
C.﹣746 kJmol﹣1
D.+746 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图向A,B中均充入1molX、1moIY,起始时A,B的体积相等都等于aL.在相同温度压强和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应:X(g)+Y(g)2Z(g)+W(g);△H<0.达平衡时,A的体积为1.4aL.下列说法错误的是( ) 
A.反应速率:v(B)>v(A)
B.A容器中X的转化率为80%
C.平衡时的压强:PB=PA
D.平衡时向A容器中充入与反应无关的气体M,能减慢A容器内化学反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:报据下列有关图象,回答有关问题:
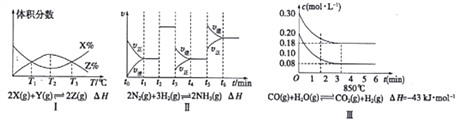
(1)由图I知,该反应的△H__________0(填“>”或“<”〉)
(2)由图Ⅱ知,反应在________时刻,NH3体枳分数最大(填t1~t2或t2~t3或t3~t4或t4~t5或t5~t6)
(3)图Ⅲ表示在10L容器、850℃时的反应,由图知,到4min时,反应放出的热量为___________。
Ⅱ: 25℃时,将体积为Va、pH=ɑ的某一元强酸与体积为Vb、pH=b的某一元强碱混合,且己知ɑ=0.56,
Va请完成下列各题。
(1)ɑ是否可以等于3 (填“是”或“否”)____________。
(2)若a+b=13,酸是盐酸,碱是KOH,现用盐酸滴定50.00mLKOH溶液,当滴定到溶液的pH=2时,消耗盐酸11.11mL。则b=___________。
(3)若己知酸是强酸,碱是强碱,酸和碱恰好中和,则ɑ的取值范围是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
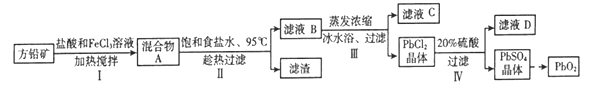
【题目】铅蓄电池有广泛的应用,由方铅矿(PbS)制备铅蓄电池电极材料(PbO2)的方法如下:
査阅资料:①PbCl2(s)+2Cl-(aq) ![]() PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
②Fe3+、Pb2+以氢氧化物形式开始沉淀时的PH值分别为1.9、7.0
③不同温度和浓度的食盐溶液中PbCl2的溶解度(g L-1):
| 20 | 40 | 60 | 100 | 180 | 260 | 300 |
13 | 3 | 1 | 0 | 0 | 3 | 9 | 13 |
50 | 8 | 4 | 3 | 5 | 10 | 21 | 35 |
100 | 17 | 11 | 12 | 15 | 30 | 65 | 95 |
(1)步骤I中FeCl3溶液与PbS反应生成PbCl2和S的化学方程式为__________________;
加入盐酸控制pH小于1.0的原因是________。
(2)步骤II中浸泡溶解时采用95℃和饱和食盐水的目的分别是____________、_____________。
(3)步骤III中将滤液B蒸发浓缩后再用冰水浴的原因是___________(请用平衡移动原理解释)。
(4)骤IV需用溶质质量分数为20%、密度为1.22 g·cm-3的硫酸溶液,现用溶质质量分数为98.3%、密度为1.84 g·cm-3的浓硫酸配制,需用到的玻璃仪器有___________ (填相应的字母)。
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒 F.胶头滴管
(5)用铅蓄电池为电源,采用电解法分开处理含有Cr2O72-及含有NO2-的酸性废水(最终Cr2O72-转化为Cr(OH)3, NO2-转化为无毒物质),其装置如下图所示。
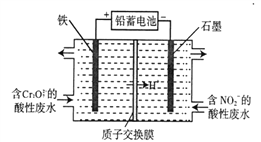
①左池中Cr2O72-转化为Cr3+的离子方程式是__________________。
②当阴极区消耗2 mol NO2-时,右池减少的H+的物质的量为______________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com