
”¾ĢāÄæ”æŌŚČŻ»żĪŖ2.0 LµÄĆܱÕČŻĘ÷ÄŚ£¬ĪļÖŹDŌŚT ”ꏱ·¢Éś·“Ó¦£¬Ęä·“Ó¦ĪļŗĶÉś³ÉĪļµÄĪļÖŹµÄĮæĖꏱ¼ätµÄ±ä»Æ¹ŲĻµČēÓŅĶ¼£¬ĻĀĮŠŠšŹö“ķĪóµÄŹĒ£Ø £©

A. øł¾ŻÓŅĶ¼øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ![]()
B. ČōŌŚµŚ7·ÖÖÓŹ±Ōö¼ÓDµÄĪļÖŹµÄĮ棬AµÄĪļÖŹµÄĮæ±ä»ÆĒéæö·ūŗĻaĒśĻß
C. ČōŌŚµŚ5·ÖÖÓŹ±ÉżøßĪĀ¶Č£¬ŌņøĆ·“Ó¦µÄÕż·“Ó¦ŹĒĪüČČ·“Ó¦£¬·“Ó¦µÄĘ½ŗā³£ŹżŌö“ó£¬BµÄ·“Ó¦ĖŁĀŹŌö“ó
D. “Ó·“Ó¦æŖŹ¼µ½µŚŅ»“Ī“ļµ½Ę½ŗāŹ±£¬AĪļÖŹµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0. 067mol/(L”¤min)
”¾“š°ø”æB
”¾½āĪö”æĘ½ŗāŹ±DµÄĪļÖŹµÄĮæ¼õÉŁĮĖ0.4mol£¬AµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.4mol£¬BµÄĪļÖŹµÄĮæŌö¼ÓĮĖ0.2mol£¬¼“D”¢A”¢BµÄĪļÖŹµÄĮæ±ä»ÆĮæÖ®±ČŹĒ2:2:1£¬ĖłŅŌøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2D£Øs£©![]() 2A£Øg£©£«B£Øg£©£¬øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK£½c£ØA£©2”¤c£ØB£©£¬AĻīÕżČ·£»DŹĒ¹ĢĢ壬øıä¹ĢĢåµÄÖŹĮæ£¬Ę½ŗā²»ŅĘ¶Æ£¬Ōņ±ķŹ¾AµÄĪļÖŹµÄĮæ±ä»ÆŹĒbĒśĻߣ¬BĻī“ķĪó£»ÉżøßĪĀ¶Č£¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬ŅņÕż·“Ó¦ŹĒĪüČČ·“Ó¦£¬ŌņÉżøßĪĀ¶ČĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬·“Ó¦µÄĘ½ŗā³£ŹżŌö“ó£¬CĻīÕżČ·£»“Ó·“Ó¦æŖŹ¼µ½µŚŅ»“Ī“ļµ½Ę½ŗāŹ±£¬µŚŅ»“Ī“ļµ½Ę½ŗāŹ±£¬AĪļÖŹŌö¼ÓĮĖ0.4mol£¬ŌņAµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ
2A£Øg£©£«B£Øg£©£¬øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK£½c£ØA£©2”¤c£ØB£©£¬AĻīÕżČ·£»DŹĒ¹ĢĢ壬øıä¹ĢĢåµÄÖŹĮæ£¬Ę½ŗā²»ŅĘ¶Æ£¬Ōņ±ķŹ¾AµÄĪļÖŹµÄĮæ±ä»ÆŹĒbĒśĻߣ¬BĻī“ķĪó£»ÉżøßĪĀ¶Č£¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬ŅņÕż·“Ó¦ŹĒĪüČČ·“Ó¦£¬ŌņÉżøßĪĀ¶ČĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬·“Ó¦µÄĘ½ŗā³£ŹżŌö“ó£¬CĻīÕżČ·£»“Ó·“Ó¦æŖŹ¼µ½µŚŅ»“Ī“ļµ½Ę½ŗāŹ±£¬µŚŅ»“Ī“ļµ½Ę½ŗāŹ±£¬AĪļÖŹŌö¼ÓĮĖ0.4mol£¬ŌņAµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ![]() 0.067mol/£ØL”¤min£©£¬DĻīÕżČ·”£
0.067mol/£ØL”¤min£©£¬DĻīÕżČ·”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCuSO4ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ÓŠ¹ŲÖʱøĶ¾¾¶¼°ŠŌÖŹČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
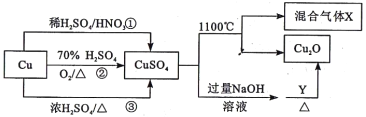
A. Ķ¾¾¶¢ŁĖłÓĆ»ģĖįÖŠH2SO4ÓėHNO3ĪļÖŹµÄĮæÖ®±Č×īŗĆĪŖ3:2
B. Éś³ÉµČĮæµÄĮņĖįĶ,ČżøöĶ¾¾¶ÖŠ²Ī¼Ó·“Ó¦µÄĮņĖįµÄĪļÖŹµÄĮæ: ¢Ł=¢Ś<¢Ū
C. ĮņĖįĶŌŚ1100”ę·Ö½āµÄ·½³ĢŹ½ĪŖ:2CuSO4![]() Cu2O+SO2”ü+SO3”ü+O2”ü
Cu2O+SO2ӟ+SO3ӟ+O2ӟ
D. µ±YĪŖĘĻĢŃĢĒŹ±£¬ĘĻĢŃĢĒ·¢Éś»¹Ō·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææĘѧ¼Ņ»ż¼«Ģ½Ė÷ŠĀ¼¼Źõ¶ŌCO2½ųŠŠ×ŪŗĻĄūÓĆ”£
¢ń£®CO2æÉÓĆĄ“ŗĻ³ÉµĶĢ¼Ļ©Ģž£ŗ2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ”÷H=akJ/mol
CH2=CH2(g)+4H2O(g) ”÷H=akJ/mol
Ēė»Ų“š£ŗ
£Ø1£©ŅŃÖŖ£ŗH2ŗĶCH2=CHµÄČ¼ÉÕČČ·Ö±šŹĒ285.8kJ/molŗĶ1411.0kJ/mol£¬ĒŅH2O(g)![]() H2O(£Ø1£©”÷H=-44.0kJ/mol£¬Ōņa=________kJ/mol”£
H2O(£Ø1£©”÷H=-44.0kJ/mol£¬Ōņa=________kJ/mol”£
£Ø2£©ÉĻŹöÓÉCO2ŗĻ³ÉCH2=CH2µÄ·“Ó¦ŌŚ________ĻĀ×Ō·¢½ųŠŠ(Ģī”°øßĪĀ”±»ņ”°µĶĪĀ”±)”£
£Ø3£©ŌŚĢå»żĪŖ1LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ£¬³äČė3molH2ŗĶ1molCO2£¬²āµĆĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹŗĶ“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°ĻģČēĶ¼1ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ________”£
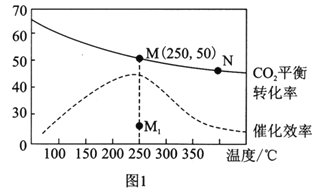
A£®Ę½ŗā³£Źż“󊔣ŗKMN
B£®ĘäĖūĢõ¼ž²»±ä,Čō²»Ź¹ÓĆ“ß»Æ¼Į£¬Ōņ250”ꏱCO2µÄĘ½ŗā×Ŗ»ÆĀŹæÉÄÜĪ»ÓŚµćM1
C£®Ķ¼1ÖŠMµćŹ±,ŅŅĻ©µÄĢå»ż·ÖŹżĪŖ7.7%
D£®µ±Ń¹Ēæ»ņn(H2)/n(CO2)²»±äŹ±¾łæÉÖ¤Ć÷»Æѧ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬
£Ø4£©±£³ÖĪĀ¶Č²»±ä,ŌŚĢå»żĪŖV LµÄŗćČŻČŻĘ÷ÖŠŅŌn(H2)”Ćn(CO2)=3”Ć1µÄĶ¶ĮĻ±Č¼ÓČė·“Ó¦Īļ,t0Ź±“ļµ½»ÆŃ§Ę½ŗā”£ĒėŌŚĶ¼2ÖŠ×÷³öČŻĘ÷ÄŚ»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ![]() Ėꏱ¼ä±ä»ÆµÄĶ¼Ļó”£___________
Ėꏱ¼ä±ä»ÆµÄĶ¼Ļó”£___________
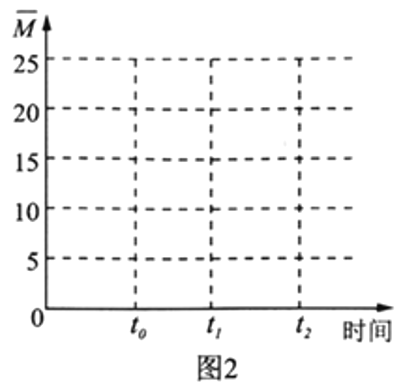
¢ņ£®ĄūÓĆ”°Na-CO2”±µē³Ų½«CO2±ä·ĻĪŖ±¦”£ĪŅ¹śæĘŃŠČĖŌ±ŃŠÖĘ³öµÄæɳäµē”°Na-CO2”±µē³Ų,ŅŌÄĘ²ŗĶ¶ą±ŚĢ¼ÄÉĆ×¹Ü(MWCNT)ĪŖµē¼«²ÄĮĻ,×Ü·“Ó¦ĪŖ4Na+3CO2![]() 2Na2CO3+C”£·ÅµēŹ±øƵē³Ų”°ĪüČė”±CO2,Ę乤×÷ŌĄķČēĶ¼3ĖłŹ¾£ŗ
2Na2CO3+C”£·ÅµēŹ±øƵē³Ų”°ĪüČė”±CO2,Ę乤×÷ŌĄķČēĶ¼3ĖłŹ¾£ŗ
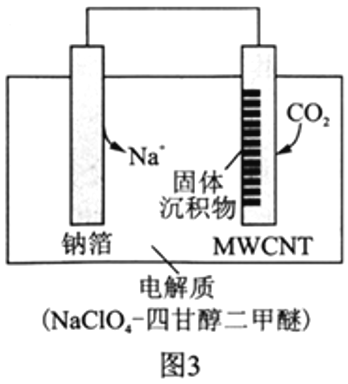
£Ø5£©·ÅµēŹ±,Õż¼«µÄµē¼«·“Ó¦Ź½ĪŖ__________________”£
£Ø6£©ČōÉś³ÉµÄNa2CO3ŗĶCČ«²æ³Į»żŌŚÕż¼«±ķĆę£¬µ±×ŖŅĘ0.2mole-Ź±£¬Õż¼«Ōö¼ÓµÄÖŹĮæĪŖ_______g”£
£Ø7£©Ń”ÓĆøßĀČĖįÄĘĖÄøŹ“¼¶ž¼×ĆŃ×öµē½āŅŗµÄÓŵćŹĒ_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŹµŃéŹŅŠčŅŖ0.2mol/L NaOHČÜŅŗ500mLŗĶ0.5mol/LĮņĖįČÜŅŗ450mL£®øł¾ŻÕāĮ½ÖÖČÜŅŗµÄÅäÖĘĒéæö»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČēĶ¼ĖłŹ¾µÄŅĒĘ÷ÖŠÅäÖĘČÜŅŗæĻ¶Ø²»ŠčŅŖµÄŹĒ________£ØĢīŠņŗÅ£©£¬ÅäÖĘÉĻŹöČÜŅŗ»¹ŠčÓƵ½µÄ²£Į§ŅĒĘ÷ŹĒ________£ØĢīŅĒĘ÷Ćū³Ę£©£®
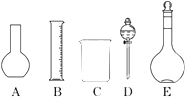
£Ø2£©ČŻĮæĘæŹĒÅäÖĘČÜŅŗµÄÖ÷ŅŖŅĒĘ÷£¬ČŻĮæĘæÉĻ±źÓŠŅŌĻĀĮłĻīÖŠµÄ________£ØĢīŠ“ŠņŗÅ£©£®
¢ŁĪĀ¶Č ¢ŚÅØ¶Č ¢ŪČŻĮæ ¢ÜŃ¹Ēæ ¢ŻĖįŹ½»ņ¼īŹ½ ¢ŽæĢ¶ČĻß
£Ø3£©ÅäÖĘŹ±£¬ĘäÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ£ØÓĆ×ÖÄø±ķŹ¾£¬Ćæøö×ÖÄøÖ»ÄÜÓĆŅ»“Ī£©________£®
A£®ÓĆ30mLĖ®Ļ“µÓÉÕ±2”«3“Ī£¬Ļ“µÓŅŗ¾ł×¢ČėČŻĮæĘæ
B£®×¼Č·³ĘČ”¼ĘĖćĮæµÄĒāŃõ»ÆÄĘ¹ĢĢåÓŚÉÕ±ÖŠ£¬ŌŁ¼ÓČėÉŁĮæĖ®£ØŌ¼50mL£©£¬ÓĆ²£Į§°ōĀżĀż½Į¶Æ£¬Ź¹Ęä³ä·ÖČܽā£¬ĄäČ“µ½ŹŅĪĀ
C£®½«ČŻĮæĘæøĒ½ō£¬Ņ”ŌČ
D£®½«ČܽāµÄĒāŃõ»ÆÄĘČÜŅŗŃŲ²£Į§°ō×¢ČėČŻĮæĘæÖŠ
E£®øÄÓĆ½ŗĶ·µĪ¹Ü¼ÓĖ®£¬Ź¹ČÜŅŗ°¼ŅŗĆęĒ”ŗĆÓėæĢ¶ČĻąĒŠ
F£®¼ĢŠųĶłČŻĮæĘæÄŚŠ”ŠÄ¼ÓĖ®£¬Ö±µ½ŅŗĆę½Ó½üæĢ¶Č2”«3cm“¦
£Ø4£©øł¾Ż¼ĘĖć£¬ÅäÖĘ0.2mol/L NaOHČÜŅŗ500mLŠč NaOH¹ĢĢåµÄÖŹĮæĪŖ£ŗ________g£®
£Ø5£©ÅäÖĘ¹ż³ĢÖŠŠčĻČŌŚÉÕ±ÖŠ½«ÅØĮņĖį½ųŠŠĻ”ŹĶ£¬Ļ”ŹĶŹ±²Ł×÷·½·ØŹĒ£ŗ________£®
£Ø6£©½«ĖłÅäÖʵÄĻ”H2SO4½ųŠŠ²ā¶Ø£¬·¢ĻÖŹµ¼ŹÅØ¶ČŠ”ÓŚ0.5mol/L£®ĒėÄć·ÖĪöĻĀĮŠÄÄŠ©²Ł×÷»įŅżĘšĖłÅäÅضČĘ«Š”£ØĢīŠ“×ÖÄø£©_______ £®
A.ÓĆĮæĶ²ĮæČ”ÅØĮņĖįŹ±£¬ŃöŹÓĮæĶ²µÄæĢ¶Č
B.ČŻĮæĘæĪ“øÉŌļ¼“ÓĆĄ“ÅäÖĘČÜŅŗ
C.ÅØĮņĖįŌŚÉÕ±ÖŠĻ”ŹĶŗó£¬Ī“ĄäČ“¾ĶĮ¢¼“×ŖŅʵ½ČŻĮæĘæÖŠ£¬²¢½ųŠŠ¶ØČŻ
D.ĶłČŻĮæĘæ×ŖŅĘŹ±£¬ÓŠÉŁĮæŅŗĢ彦³ö
E.ŌŚČŻĮæĘæÖŠ¶ØČŻŹ±ø©ŹÓČŻĮæĘææĢ¶ČĻß
F.ÉÕ±Ī“½ųŠŠĻ“µÓ
G.¶ØČŻŗóČūÉĻĘæČū·“ø“Ņ”ŌČ£¬¾²ÖĆŗó£¬ŅŗĆę²»µ½æĢ¶ČĻߣ¬ŌŁ¼ÓĖ®ÖĮæĢ¶ČĻߣ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŹ³Ę·øÉŌļ¼ĮµÄÖ÷ŅŖ³É·ÖŹĒŃõ»ÆøĘ£®Ńõ»ÆøĘ£ØCaO£©Ó¦ŹōÓŚ£Ø £©
A.Ėį
B.¼ī
C.ŃĪ
D.Ńõ»ÆĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČżĀČŃõĮ×(POCl3)ŹĒÖŲŅŖµÄ»ł“”»Æ¹¤ŌĮĻ£¬¹ć·ŗÓĆÓŚÖĘŅ©”¢Č¾»Æ”£ĖܽŗÖś¼ĮµČŠŠŅµ”£Ä³ŠĖȤŠ”×éÄ£ÄāPCl3Ö±½ÓŃõ»Æ·ØÖʱøPOCl3,ŹµŃé×°ÖĆÉč¼ĘČēĻĀ:

ÓŠ¹ŲĪļÖŹµÄ²æ·ÖŠŌÖŹČēĻĀ±ķ:
ČŪµć/”ę | ·Šµć/”ę | ĘäĖū | |
PCl3 | -112 | 75.5 | ÓöĖ®Éś³ÉH3PO3ŗĶHCl£¬ÓöO2Éś³ÉPOCl3 |
POCl3 | 2 | 105.3 | ÓöĖ®Éś³ÉH3PO4ŗĶHCl,ÄÜČÜÓŚPCl3 |
»Ų“šĻĀĮŠĪŹĢā:
(1)ŅĒĘ÷aµÄĆū³ĘŹĒ_____£¬×°ÖĆAÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________”£
(2)B×°ÖƵÄ×÷ÓĆ³ż¹Ū²ģO2µÄĮ÷ĖŁÖ®Ķā”£»¹ÓŠ____________”£
(3)C×°ÖĆæŲÖĘ·“Ó¦ŌŚ60”ꔫ65”ę½ųŠŠ£¬ĘäÖ÷ŅŖÄæµÄŹĒ____________”£
(4)Ķعż·š¶ū¹žµĀ·ØæÉŅŌ²ā¶ØČżĀČŃõĮײśĘ·ÖŠClŌŖĖŲŗ¬Į棬ŹµŃé²½ÖčČēĻĀ:
I.Č”xg²śĘ·ÓŚ×¶ŠĪĘæÖŠ£¬¼ÓČė×ćĮæNaOHČÜŅŗ£¬“żĶźČ«·“Ó¦ŗó¼ÓĻ”ĻõĖįÖĮĖįŠŌ”£
II.Ļņ׶ŠĪĘæÖŠ¼ÓČė0.1000mol/LµÄAgNO3ČÜŅŗ40.00mL,Ź¹Cl-ĶźČ«³Įµķ”£
III.ĻņĘäÖŠ¼ÓČė2mLĻõ»ł±½£¬ÓĆĮ¦Ņ”¶Æ£¬Ź¹³Įµķ±ķĆę±»ÓŠ»śĪļø²øĒ”£
IV.¼ÓČėÖøŹ¾¼Į£¬ÓĆcmol/LNH4SCNČÜŅŗµĪ¶Ø¹żĮæAg+ÖĮÖÕµć£¬¼ĒĻĀĖłÓĆĢå»żVmL”£
ŅŃÖŖ:Ksp(AgCl)=3.2”Į10-10,Ksp(AgSCN)=2”Į10-12
¢ŁµĪ¶ØŃ”ÓƵÄÖøŹ¾¼ĮŹĒ_______(Ģī±źŗÅ)£¬µĪ¶Ø½KµćµÄĻÖĻóĪŖ_____________”£
a.FeCl2 b.NH4Fe(SO4)2 c.µķ·Ū d.¼×»ł³Č
¢ŚC1ŌŖĖŲµÄÖŹĮæ°Ł·Öŗ¬ĮæĪŖ(ĮŠ³öĖćŹ½)____________”£
¢Ū²½ÖčIII¼ÓČėĻõ»ł±½µÄÄæµÄŹĒ___£¬ČēĪŽ“Ė²Ł×÷£¬Ėł²āC1ŌŖĖŲŗ¬Į潫»į___(Ģī”°Ę«“ó”±”°Ę«Š””±»ņ”°²»±ä”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»·¼ŗĻ©“ÖĘ·ÖŠŗ¬ÓŠ»·¼ŗ“¼ŗĶÉŁĮæĖįŠŌŌÓÖŹµČ”£¼ÓČė±„ŗĶŹ³ŃĪĖ®£¬Õńµ“”¢¾²ÖĆ”¢·Ö²ć£¬»·¼ŗĻ©ŌŚ_________²ć(Ģī"ÉĻ"»ņ"ĻĀ")£¬·ÖŅŗŗóŌŁÓĆ_________Ļ“µÓ(ĢīČė±ąŗÅ)”£ŅŃÖŖ£ŗ
ĆܶČ(g/cm3) | ČŪµć(”ę) | ·Šµć(”ę) | ČܽāŠŌ | |
»·¼ŗ“¼ | 0.96 | 25 | 161 | ÄÜČÜÓŚĖ® |
»·¼ŗĻ© | 0.81 | -103 | 83 | ÄŃČÜÓŚĖ® |
A£®KMnO4ČÜŅŗ B£®Ļ”H2SO4 C£® Na2CO3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø15·Ö£©¶žŃõ»ÆĮņŹĒÖŲŅŖµÄ¹¤ŅµŌĮĻ£¬Ģ½¾æĘäÖʱø·½·ØŗĶŠŌÖŹ¾ßÓŠ·Ē³£ÖŲŅŖµÄŅāŅ唣
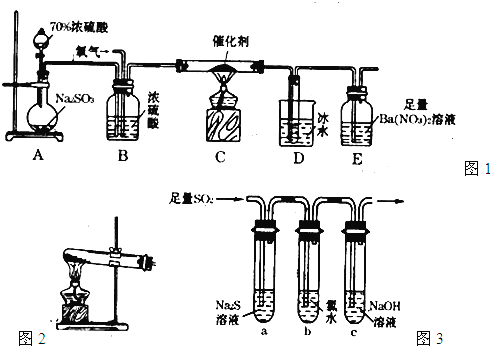
£Ø1£©ŹµŃéŹŅÓĆĶ¼1×°ÖĆ²ā¶ØSO2“ß»ÆŃõ»ÆĪŖSO3µÄ×Ŗ»ÆĀŹ”££ØŅŃÖŖSO3ČŪµćĪŖ16£®8”ę£¬¼ŁÉčĘųĢå½ųČė×°ÖĆŹ±·Ö±š±»ĶźČ«ĪüŹÕ£¬ĒŅŗöĀŌæÕĘųÖŠCO2µÄÓ°Ļģ”££©
¢Ł¼ņŹöŹ¹ÓĆ·ÖŅŗĀ©¶·ĻņŌ²µ×ÉÕĘæÖŠµĪ¼ÓÅØĮņĖįµÄ²Ł×÷£ŗ ”£
¢ŚŹµŃé¹ż³ĢÖŠ£¬ŠčŅŖĶØČėŃõĘų”£ŹŌŠ“³öŅ»øöÓĆČēĶ¼2ĖłŹ¾×°ÖĆÖĘČ”ŃõĘųµÄ»Æѧ·½³ĢŹ½£ŗ ”£
¢Ūµ±Ķ£Ö¹ĶØČėSO2ĻØĆš¾Ę¾«µĘŗ󣬊čŅŖ¼ĢŠųĶØŅ»¶ĪŹ±¼äµÄŃõĘų£¬ĘäÄæµÄŹĒ£ŗ ”£
¢ÜŹµŃé½įŹųŗó£¬Čō×°ÖĆDŌö¼ÓµÄÖŹĮæĪŖmg£¬×°ÖĆEÖŠ²śÉś°×É«³ĮµķµÄÖŹĮæĪŖng£¬Ōņ“Ė
Ģõ¼žĻĀ¶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹŹĒ £ØÓĆŗ¬×ÖÄøµÄ“śŹżŹ½±ķŹ¾£¬²»ÓĆ»Æ¼ņ£©”£
£Ø2£©Ä³Ń§Ļ°Š”×éÉč¼ĘÓĆČēĶ¼3×°ÖĆŃéÖ¤¶žŃõ»ÆĮņµÄ»ÆѧŠŌÖŹ”£
¢ŁÄÜĖµĆ÷¶žŃõ»ÆĮņ¾ßÓŠŃõ»ÆŠŌµÄŹµŃéĻÖĻóĪŖ£ŗ ”£
¢ŚĪŖŃéÖ¤¶žŃõ»ÆĮņµÄ»¹ŌŠŌ£¬³ä·Ö·“Ó¦ŗó£¬Č”ŹŌ¹ÜbÖŠµÄČÜŅŗ·ÖČż·Ż£¬·Ö±š½ųŠŠČēĻĀŹµŃ锣
·½°øI£ŗĻņµŚŅ»·ŻČÜŅŗÖŠ¼ÓČėAgNO3ČÜŅŗ£¬ÓŠ°×É«³Į
µķÉś³É”£
·½°øII£ŗĻņµŚ¶ž·ŻČÜŅŗÖŠ¼ÓČėĘ·ŗģČÜŅŗ£¬ŗģÉ«ĶŹČ„”£
·½°øIII£ŗĻņµŚČż·ŻČÜŅŗÖŠ¼ÓČėBaC12ČÜŅŗ£¬²śÉś°×É«³Įµķ
ÉĻŹö·½°øÖŠŗĻĄķµÄŹĒ £ØĢī”°I”±”¢”°II”±”¢»ņ”°III”±£©£»
ŹŌ¹Üb·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£
¢Ūµ±ĶØČė¶žŃõ»ÆĮņÖĮŹŌ¹ÜcÖŠČÜŅŗĻŌÖŠŠŌŹ±£¬øĆČÜŅŗÖŠ
c(Na+)= £ØÓĆŗ¬ĮņĪ¢Į£ÅØ¶ČµÄ“śŹżŹ½±ķŹ¾£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³Ń§ÉśµÄŹµŃé±ØøęĖłĮŠ³öµÄĻĀĮŠŹż¾ŻÖŠŗĻĄķµÄŹĒ£Ø £©
A. ÓĆĖįŹ½µĪ¶Ø¹ÜĮæČ”13.17mLĻ”ŃĪĖį
B. ÓĆ10mLĮæĶ²ĮæČ”7.13mLĻ”ŃĪĖį
C. ÓĆ¹ć·ŗpHŹŌÖ½²āµĆijČÜŅŗµÄpHĪŖ2.3
D. ÓĆĢģĘ½³ĘČ”ĪļĘ·µÄÖŹĮæĪŖ5.872g
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com