
| A、中和等体积、等物质的量浓度的盐酸和醋酸所消耗的NaOH的物质的量相等 |
| B、若NaHA溶液的pH<7,则H2A一定是强酸 |
| C、将NaOH溶液加入到NH4Cl溶液至中性时,溶液中c(NH4+)=c(Cl一) |
| D、常温下,将pH=11的Ba(OH)2溶液加水稀释10倍后,溶液的pH=12 |


科目:高中化学 来源: 题型:

| A、①③④ | B、②③④ |
| C、②③⑤ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、h1>h2>h3>h4 |
| B、h4>h3>h1>h2 |
| C、h4>h1>h3>h2 |
| D、h2>h3>h1>h4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
| c(H+) |
| c(HF) |
| c(OH-) |
| c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
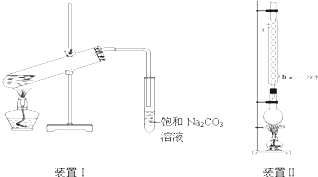
| 物 质 | 2,4,6 熔点/℃ | 沸点/℃ |
| 乙 醇 | -114 | 78 |
| 乙 酸 | 16.6 | 117.9 |
| 乙酸乙酯 | -83.6 | 77.5 |
| 98%H2SO4 | 10 | 338 |
查看答案和解析>>
科目:高中化学 来源: 题型:
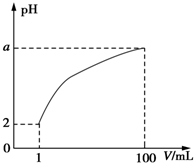 常温下,将1mL pH=2的一元酸HA溶液加水稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,将1mL pH=2的一元酸HA溶液加水稀释至100mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是( )| A、加热HA溶液时,溶液酸性增强 |
| B、1 mol?L-1 HA溶液与1 mol?L-1 NaOH溶液等体积混合,所得溶液中c(Na+)>c(A-),则2<a<4 |
| C、某浓度的NaA溶液的pH=d,则其中由水电离出的c(OH-)=1014-d mol?L-1 |
| D、HA溶液与NaOH溶液恰好完全反应时,c(Na+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com