
【题目】下列说法正确的是
A. C与Si位于同一主族,且干冰与SiO2都是酸性氧化物 ,所以二者晶体类型相同
B. NaCl和AlCl3均为强电解质,二者在熔融状态下都能导电
C. 从晶体类型上来看物质的熔沸点,其规律是:原子晶体>离子晶体>分子晶体
D. 第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】在生物体内,作为生命活动的体现者、遗传信息的携带者、膜结构的主要成分的化合物,依次为
A. 糖类、脂质、核酸 B. 蛋白质、磷脂、核酸
C. 蛋白质、糖类、核酸 D. 蛋白质、核酸、磷脂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为__________mol
(2)该气体所含原子总数为______________。
(3)该气体在标准状况下的体积为________L
(4)该气体溶于1ml水中(不考虑反应),设溶液的密度为ρg/cm3,则该溶液的物质的量浓度为_______mol· L-1。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为__________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是( )
被提纯物质 | 除杂试剂 | 分离方法 | |
A | 淀粉(NaCl) | H2O | 渗析 |
B | Al2O3(SiO2) | NaOH溶液 | 过滤 |
C | CO2(CO) | O2 | 点燃 |
D | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
①标准状况下,含NA个氩原子的氩气体积约为22.4L ②34g H2O2中含有的阴离子数为NA ③常温常压下,21g氧气和27g臭氧中含有的氧原子总数为3NA ④在Fe参与的反应中,1mol Fe失去的电子数为3NA ⑤标准状况下,11.2L的Cl2溶于水,转移的电子总数为0.5NA ⑥在O2参与的反应中,1mol O2作氧化剂时得到的电子数一定是4NA ⑦1L 1mol·L﹣1NH4NO3溶液中氮原子数小于2NA ⑧标准状况下,22.4L CCl4中所含有的分子数为NA.
A.①②⑤ B.①⑥⑧ C.①③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 1L水中溶解了58.5gNaCl,该溶液的物质的量浓度为1mol/L
B. 从1L2mol/L的H2SO4溶液中取出0.5L,该溶液溶质物质的量浓度为1mol/L
C. 0.5L2mol·L-1的BaCl2溶液中,Ba2+和Cl-的总数为3×6.02×1023
D. 10g98%的硫酸(密度为1.84g·cm-3)与10mL18.4mol·L-1的硫酸的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中c (OH-)之比为( )
A.大于10 B.小于10 C.等于10 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.稀硫酸滴在银片上:2Ag+2H+===2Ag++H2↑
B.稀硫酸与氢氧化钡溶液混合:SO![]() +Ba2+===BaSO4↓
+Ba2+===BaSO4↓
C.稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3
D.氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)![]() (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)![]() NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3 与 ΔH1、ΔH2 之间的关系是:ΔH3=________。
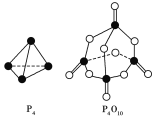
(2)白磷与氧气反应生成P4O10 固体 。下表所示是部分化学键的键能参数:
化学键 | P—P | P—O | P===O | O===O |
键能/kJ·mol-1 | a | b | c | d |
根据右图的分子结构和有关数据通过计算写出该反应的热化学方程式为 。
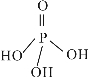
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如右下图)之间脱去两个水分子产物,其结构式为_________________,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为____________。
(4)已知298 K时白磷不完全燃烧的热化学方程式为:
P4(s,白磷)+3O2(g)===P4O6(s) ΔH=-1 638 kJ·mol-1。
在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com