
| A. | 常温下,1.8g H2O含有0.2nA个H-O共价键 | |
| B. | 1L 0.3 mol•L-1的FeCl3溶液中Fe3+数目为0.3nA | |
| C. | 标准状况下,22.4L CCl4中含 nA个CCl4分子 | |
| D. | 标准状况下,22.4L NO2和CO2的混合气体含有2nA个氧原子 |
分析 A.水分子中含有2个氧氢键,1.8g水的物质的量为0.1mol,含有0.2mol氧氢共价键;
B.铁离子部分水解,导致溶液中铁离子数目减少;
C.标况下四氯化碳不是气体,不能使用标况下的气体摩尔体积计算;
D.标况下22.4L混合气体的物质的量为1mol,1mol二氧化氮和二氧化碳的混合气体中含有2mol氧原子.
解答 解:A.1.8g H2O的物质的量为0.1mol,0.1mol水分子中含有0.2nA个H-O共价键,故A正确;
B.1L 0.3 mol•L-1的FeCl3溶液中含有溶质氯化铁0.3mol,由于铁离子部分水解,则溶液中的铁离子小于0.3mol,Fe3+数目小于0.3nA,故B错误;
C.标准状况下四氯化碳不是气体,不能使用标况下的气体摩尔体积进行计算,故C错误;
D.二氧化氮和二氧化碳分子中都含有2个氧原子,标况下22.4L二者的混合气体的物质的量为1mol,含有2mol氧原子,含有2nA个氧原子,故D正确;
故选BC.
点评 本题考查了阿伏伽德罗常的应用,侧重考查气体摩尔体积的条件应用和计算、盐的水解原理,题目难度中等,注意掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的转化关系,明确标况下气体摩尔体积的使用条件:标准状况下、气体.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:C2H4 | |
| B. | 水的电子式: | |
| C. | 氯离子的结构示意图: | |
| D. | 中子数为146,质子数为92的铀(U)原${\;}_{92}^{146}$U |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
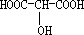 ;
;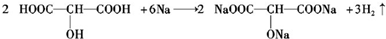 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
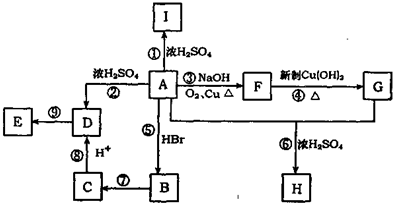
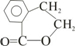 ;
;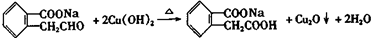 ;写出反应⑦的化学方程式
;写出反应⑦的化学方程式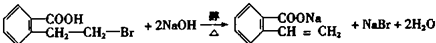 ;
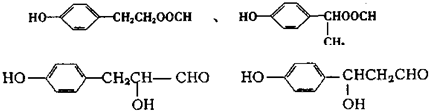
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下22.4L氯气通入足量水中反应,转移的电子数为NA | |
| B. | 乙烯和氮气组成的28g混合气体中含有NA个分子 | |
| C. | 1molNa2O2中阳离子和阴离子数均为2NA | |
| D. | 1molFeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
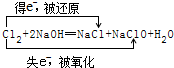
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
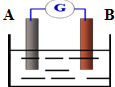 如图为某原电池装置:
如图为某原电池装置:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾起催化作用 | B. | 硫酸铝钾比碳酸氢钠更易分解 | ||
| C. | 明矾受热分解放出气体 | D. | 铝盐在水中能起到酸的作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com