
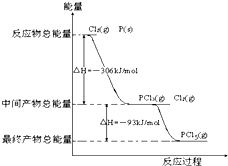
 红磷P(s)和Cl2(g)发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据),根据图回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3和PCl5,反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据),根据图回答下列问题:| 分解量 |
| 起始量 |
| 0.2mol |
| 0.8mol |
| 3 |
| 2 |
| 5 |
| 2 |


科目:高中化学 来源: 题型:
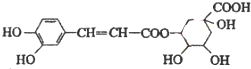
| A、分子式为C16H15O9 |
| B、不能与NaHCO3溶液反应 |
| C、能发生取代反应和消去反应 |
| D、1 mol绿原酸最多与可8mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (Ⅰ)乙苯的结构简式可以表示为
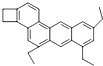
(Ⅰ)乙苯的结构简式可以表示为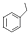 ,下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”.
,下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸中滴加氨水至中性,溶质为氯化铵 |
| B、稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小 |
| C、饱和石灰水中加入少量CaO,恢复至原温后溶液的pH值不变 |
| D、向沸水中滴加适量饱和FeCl3溶液,可制得红褐色带电的胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,有CO32-或HCO3-中的一种或两种 |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C、加入硝酸酸化的硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当n=2时,物质A、B的转化率之比为1:2 | ||
B、起始时刻和达到平衡后容器中的压强比为(1+n):(1+n-
| ||
| C、当v(A)正=2v(C)逆时,可断定反应达到平衡 | ||
| D、若起始时放入3molA和3n molB,则达到平衡时生成3a mol的C |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com