
分析 (1)计算空气中氧气的体积,利用差量法计算反应后气体体积变化,据此解答;
(2)令空气的物质的量为1mol,设设反应生成的SO2物质的量为xmol,利用差量法计算反应后气体体积变化,进而计算反应后的总体积,根据SO2的体积分数列方程计算x的值,再结合化学方程式计算出反应后氧气的物质的量,最后根据体积分数定义计算.
解答 解:(1)55L空气中氧气的体积=55L×0.2=11L,则:
4FeS2+11O2=8SO2+2Fe2O3 气体体积减少△V
11 11-8=3
11L 3L
故反应后气体的体积为55L-3L=52L,
故答案为:52;
(2)令空气的物质的量为1mol,设反应生成的SO2物质的量为xmol,则:
4FeS2+11O2=8SO2+2Fe2O3 气体物质的量减少△n
8 11-8=3
xmol $\frac{3}{8}$xmol
故反应后气体的物质的量=1mol-$\frac{3}{8}$xmol,
故$\frac{xmol}{1mol-\frac{3}{8}xmol}$=0.08,解得x=0.078,
则反应后氧气的物质的量为1mol×$\frac{1}{5}$-$\frac{11}{8}$×0.078mol=0.093mol,
反应后气体的物质的量为1mol-$\frac{3}{8}$×0.078mol=0.97mol,
因此所得混合气体中O2的体积分数为$\frac{0.093mol}{0.93mol}$×100%=9.6%,
故答案为:9.6%.
点评 本题考查根据方程式的计算,注意利用差量法计算的计算,难度中等,其中(2)计算过程较为复杂,计算过程中数据不是很整,要求计算结果的准确性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | L与Q形成的化合物化学式为LQ | |
| B. | L、M的单质与稀盐酸反应剧烈程度:M>L | |
| C. | Q、T的氢化物在常温常压下均为无色气体 | |
| D. | M的最高价氧化物的水化物不具有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 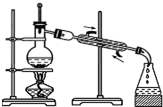 分离沸点相差较大液体混合物 | B. | 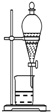 分离互不相溶的两种液体 | ||
| C. | 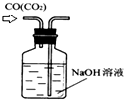 除去CO气体中的CO2气体 | D. | 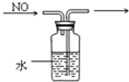 排水集气法收集NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO3溶液中存在:c(Na+)>c(HSO3-)>c(OH-)>c(H+)>c(SO32-) | |
| B. | 当吸收液呈中性时:c(Na+)=2c(SO32-)+c(HSO3-) | |
| C. | 含等物质的量的Na2SO3和NaHSO3的溶液中,阴离子数目相等 | |
| D. | Na2SO3和NaHSO3都能抑制水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Si→SiO2→H2SiO3→Na2SiO3 | |
| B. | Al→Al2O3→Al(OH)3→NaAlO2 | |
| C. | Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3 | |
| D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com