
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) +Y(g)![]() 2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) △H<0,—段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法不正确的是
A. 反应前2min的平均速率v(Z)=4.0×10-3mol/(L·min)
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)<v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【答案】D
【解析】试题分析:由题中信息可知,反应在第7分钟处于化学平衡状态。依据平衡时Y的变化量为0.06mol,求出各物质的平衡浓度依次为c(X)=0.01mol/L、c(Y)=0.01mol/L、c(Z)=0.012mol/L。A. 反应前2min的平均速率v(Z)=2 v(Y)=2![]() =4.0×10-3mol/(L·min),A正确;B. 该反应为放热反应,其他条件不变,降低温度,化学平衡向正反应方向移动,反应达到新平衡前v(逆)<v(正),B正确;C. 该温度下此反应的平衡常数K=
=4.0×10-3mol/(L·min),A正确;B. 该反应为放热反应,其他条件不变,降低温度,化学平衡向正反应方向移动,反应达到新平衡前v(逆)<v(正),B正确;C. 该温度下此反应的平衡常数K=![]() =1.44,C正确;D. 该反应前后气体的分子数不变,所以改变压强后,平衡不移动。其他条件不变,再充入0.2molZ,相当于对原平衡加压,所以平衡时X的体积分数不变,D不正确。本题选D。
=1.44,C正确;D. 该反应前后气体的分子数不变,所以改变压强后,平衡不移动。其他条件不变,再充入0.2molZ,相当于对原平衡加压,所以平衡时X的体积分数不变,D不正确。本题选D。


科目:高中化学 来源: 题型:
【题目】向2L的密闭容器中充入7.6mol NO和3.8mol O2 , 发生如下反应: ①2NO(g)+O2(g)2NO2(g)
②2NO2(g)N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )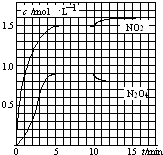
A.前5min反应的平均速率v(N2O4)=0.36mol(Lmin)﹣1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , T1℃达到平衡时,N2O4的转化率为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 甲烷和氯气光照条件下发生取代反应后,得到的有机产物有5种
B. 乙烷中混有的少量乙烯,可通入氢气让乙烯和氢气发生加成反应来除去乙烯
C. 乙烯和乙炔都能使溴水褪色,但可通过燃烧现象的不同来区别它们
D. 氨基酸、蛋白质在一定条件下都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“洁净煤技术”研究在世界上相当普遍.
(1)科研人员通过向地下煤层(焦炭)气化炉中鼓入水蒸气的方法,连续产出了高热值 的煤炭气,其主要成分是CO和H2 .
已知:H2(g)+ ![]() O2(g)═H2O(g)△H1=﹣241.8kJmol﹣1
O2(g)═H2O(g)△H1=﹣241.8kJmol﹣1
C(s)+ ![]() O2(g)═CO(g)△H2=﹣110.5kJmol﹣1
O2(g)═CO(g)△H2=﹣110.5kJmol﹣1
则生产煤炭气的热化学方程式为
(2)CO在催化剂作用下可以与H2反应生成甲醇:CO(g)+2H2(g)CH3OH(g). 在2L密闭容器中充有10mol CO与20mol H2 , CO的平衡转化率与温度、压强的关系如图所示.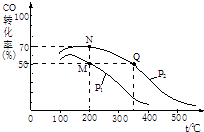
①关于上述反应在化学平衡状态时的描述正确的是 .
A.CO的含量保持不变
B.v正(CO)=v正(CH3OH)
C.容器中混合气体的平均相对分子质量保持不变
②该图像中P1P2(填“>”、“=”或“<”);
该反应逆反应的△H0 (填“>”、“=”或“<”).
③该反应的化学平衡常数表达式为K= , M、N、Q三点的平衡常数KM、KN、KQ的大小关系为 .
④M,N两点平衡状态下,容器中总物质的量之比为:n(M)总:n(N)总= .
(3)已知在常温常压下: ①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H=﹣1275.6kJ/mol
②2CO(g)+O2(g)═2CO2(g)△H=﹣566.0kJ/mol
③H2O(g)═H2O(l)△H=﹣44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 向鸡蛋清的溶液中加入浓的硫酸铵溶液,蛋白质的性质发生改变并凝聚
B. 将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,下层析出肥皂
C. 油脂为髙分子化合物,分子结构中都含有酯基
D. 纤维素、麦芽糖在一定条件下均可转化为葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列每组物质发生状态变化所克服的粒子间的相互作用属于同种类型的是
A. 食盐和蔗糖熔化 B. 钠和硫熔化
C. 碘和干冰升华 D. 二氧化硅和氧化钠熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是( ) 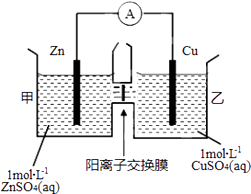
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42﹣)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com