
| A. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-121.5kJ•mol-1 | |
| B. | 2CO2(g)+3H2(g)═$\frac{1}{2}$CH3OCH3(g)+$\frac{3}{2}$H2O(g)△H=-25.5kJ•mol-1 | |
| C. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=+121.5kJ•mol-1 | |
| D. | 2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-72.5kJ•mol-1. |
分析 由①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1,
结合盖斯定律可知,①×②+②得到2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g),以此来解答.
解答 解:由①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,
②2CH3OH(g)═CH3OCH3(g)+H2O(g)△H=-23.5kJ•mol-1,
结合盖斯定律可知,①×②+②得到2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g),则△H=(-49.0kJ•mol-1)×2+(-23.5kJ•mol-1)=-121.5kJ•mol-1,
即CO2与H2反应合成二甲醚的热化学方程式为2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-121.5kJ•mol-1,
故选A.
点评 本题考查热化学方程式,为高频考点,把握已知反应与目标反应的关系为解答的关键,侧重分析与应用能力的考查,注意盖斯定律的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
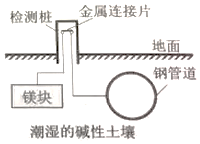
| A. | 该方法是将化学能转化成了电能 | |
| B. | 在此装置中钢管道做负极 | |
| C. | 该方法称为“外加电流阴极保护法” | |
| D. | 镁块上发生的电极反应:O2+2H2O+4e→4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 李白诗句“日照香炉生紫烟,遥看瀑布挂前川”,“紫烟”指“香炉”中碘升华的现象 | |
| B. | 刘禹锡诗句“千淘万漉虽辛苦,吹尽狂沙始到金”,金性质稳定,可通过物理方法得到 | |
| C. | 王安石诗句“爆竹声中一岁除,春风送暖入屠苏”,爆竹的燃放涉及氧化还原反应 | |
| D. | 曹植诗句“煮豆燃豆萁,豆在釜中泣”,这里的能量变化主要是化学能转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作和现象 | 结论 |
| A | 将表面附有黑色Ag2S的银器浸入盛有食盐水的铝质容器中,黑色逐渐褪去 | 银器为正极,Ag2S得电子生成单质银 |
| B | 测定相同浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 非金属性:S>C |
| C | 向NaAlO2溶液中滴入NaHCO3溶液,有白色沉淀生成 | AlO2-和HCO3-的水解反应相互促进 |
| D | 将Fe(NO3)2晶体溶于稀H2SO4后,滴加KSCN溶液,溶液变红 | Fe(NO3)2晶体已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子排布为1s22s22p43s2的原子处于激发态 | |
| B. | 某元素质量数51,中子数28,其基态原子中未成对电子数为1 | |
| C. | 若某基态原子的外围电子排布为4d15s2,该元素原子核外有5个电子层 | |
| D. | BF3中B原子sp2杂化,为平面三角形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可能存在核外电子排布式为1s22s22p63s23p64s24p1的原子 | |
| B. | 当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,而且自旋方向相反 | |
| C. | 次氯酸的电子式:H?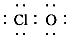 | |
| D. | 基态原子的电子获得一定能量变为激发态原子,而激发态原子变为基态原子,则要放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L氧气所含的原子数为NA | |
| B. | 2.3g金属钠变为钠离子得到0.1NA电子 | |
| C. | 0.5mol/LH2SO4中的H+数为NA | |
| D. | 常温常压下32g O2与O3的混合物含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com