
【题目】下列关于![]() 晶体网状结构(如图)的叙述正确的是
晶体网状结构(如图)的叙述正确的是
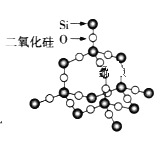
A. 存在四面体结构单元, ![]() 处于中心,
处于中心, ![]() 处于4个顶角
处于4个顶角
B. 最小环上有3个![]() 原子和3个
原子和3个![]() 原子
原子
C. 最小环上![]() 和
和![]() 原子数之比为1:2
原子数之比为1:2
D. 最小环上有6个![]() 原子和6个
原子和6个![]() 原子
原子
科目:高中化学 来源: 题型:
【题目】由甲醇![]() 、氧气和
、氧气和![]() 溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
(1)写出该电池负极电极反应式______
(2)若以该电池为电源,用石墨作电极电解含有如下离子的溶液。
离子 |
|
|
|
|
|
|
|
|
|
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上发生的电极反应为______;阴极收集到的气体体积为(标准状况)______。
(3)若用该电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移![]() 时,实际上消耗的甲醇的质量比理论上大,可能原因是______。
时,实际上消耗的甲醇的质量比理论上大,可能原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子序数依次增大。m、n、r为这些元素组成的化合物,常温下,0.1 mol·L-1 m溶液的pH=13,组成n的两种离子的电子层数相差1。p、q为其中两种元素形成的单质。上述物质的转化关系如图所示。下列说法正确的是 ( )
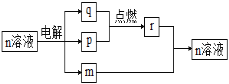
A. 原子半径:X<Y<Z<W
B. X、Z既不同周期也不同主族
C. 简单氢化物的沸点:Y<W
D. Y、Z、W形成的一种化合物具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“循环经济”和“低碳经济”是目前备受关注的课题,因而对碳和硫的化合物的综合利用成为研究的热点。请回答下列问题:
(1)下列事实中,不能用来比较碳元素和硫元素非金属性强弱的是______(填选项字母)。
A.![]() 有漂白性而
有漂白性而![]() 没有
没有
B.少量![]() 能与
能与![]() 反应生成
反应生成![]()
C.![]() 能使酸性
能使酸性![]() 溶液褪色而
溶液褪色而![]() 不能
不能
D.![]() 溶液显碱性而
溶液显碱性而![]() 溶液显中性
溶液显中性
(2)下图是通过热循环进行能源的综合利用和污染治理的反应系统原理。

系统(Ⅱ)制氢气的热化学方程式为_________;两个系统制得等量的H2所需能量较少的是________。
(3)向10 L恒容密闭容器中充入2 mol CO和1 mol ![]() ,发生反应2CO(g)+SO2 (g)
,发生反应2CO(g)+SO2 (g)![]() S(g)+2CO2 (g)。CO和CO2的平衡体积分数(φ)与温度(T)的关系如图所示。
S(g)+2CO2 (g)。CO和CO2的平衡体积分数(φ)与温度(T)的关系如图所示。
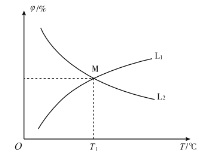
①图中能表示CO的平衡体积分数与温度关系的曲线为______(填“L1”或“L2”)。
②T1 ℃时,![]() 的平衡转化率α1=_______,反应的平衡常数
的平衡转化率α1=_______,反应的平衡常数![]() _________。
_________。
③只改变下列条件,既能加快该反应速率,又能增大CO的平衡转化率的是_____(填选项字母)。
A.增大压强 B.充入一定量![]()
C. 充入一定量![]() D.加入适当催化剂
D.加入适当催化剂
④向起始温度为![]() ℃的10 L绝热容器中充入2 mol CO和1 mol
℃的10 L绝热容器中充入2 mol CO和1 mol ![]() ,重复实验,该反应的平衡常数
,重复实验,该反应的平衡常数![]() _____
_____![]() (填“>”“<”或“=”),理由为_____。
(填“>”“<”或“=”),理由为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅹ、Y、Z、W、M五种元素的原子序数依次增大。已知Ⅹ、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。下列说法正确的是
A. 原子半径:r(M)>r(Y)>r(Z)>r(W)>r(X)
B. W和M形成的化合物不能与强碱反应
C. Ⅹ、Z、W三元素所形成的化合物一定为共价化合物
D. Y、Z的最高价含氧酸的酸性:Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若![]() 与
与![]() 的电子层结构相同,且2个
的电子层结构相同,且2个![]() 原子与3个
原子与3个![]() 原子的电子总数相等,则下列说法正确的是
原子的电子总数相等,则下列说法正确的是
A. ![]() 为硫元素
为硫元素
B. ![]() 元素原子的外围电子排布式为
元素原子的外围电子排布式为![]()
C. ![]() 元素原子的核外电子排布式为
元素原子的核外电子排布式为![]()
D. ![]() 、
、![]() 都是元素周期表中
都是元素周期表中![]() 区的元素
区的元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物K是某药物的前体,合成路线如图所示:
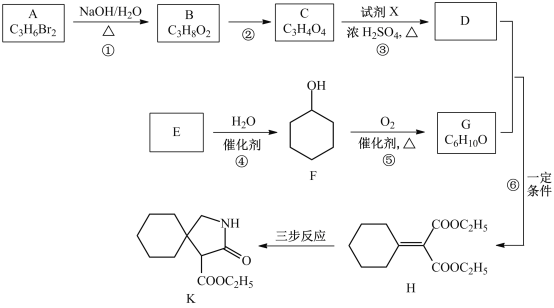
已知:R-CN![]()
![]() ;
;
![]()
![]() +
+![]()
(1)A的名称是_____________。
(2)反应①的化学方程式是___________________。
(3)反应②的类型是__________________。
(4)反应③中的试剂X是________________。
(5)E属于烃,其结构简式是_________________。
(6)H中所含的官能团是_________________。
(7)反应⑥的化学方程式是_____________________。
(8)H经三步反应合成K,写出中间产物I和J的结构简式______________。
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国政府承诺到2020年单位GDP二氧化碳排放比2005年下降40%~45%。CO2可转化成有机物实现碳循环。在体积为1L的密闭容器中充入1mol CO2和3mol H2,一定条件下发生反应:![]() ,测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
,测得CO2和CH3OH(g)的浓度随时间的变化如图所示。

(1)3~9min内,v(H2)=_________mol·L-1·min-1。
(2)能说明上述反应达到平衡状态的是________(填序号)。
A.反应中CO2与CH3OH的物质的量浓度之比为l:1(即图中交点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3mol H2,同时生成1mol CO2
D. CO2的体积分数在混合气体中保持不变
(3)平衡时CO2的转化率为________
(4)平衡时混合气体中CH3OH(g)的体积分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)![]() H、
H、![]() H、
H、![]() H互为__;O2、O3互为__。
H互为__;O2、O3互为__。
(2)在下列固体中:a.CaCl2 b.KOH c.He d.H2SO4 e.NH4Cl f.金刚石
①其中不含化学键的物质是__。
②既含有离子键又含有共价键的物质是__(填序号)。
(3)如图是几种常见的电池装置。请回答:

①电池Ⅰ中负极反应式是__,溶液中H+向__(填“负”或“正”)极移动,若1mol电子流过导线,则产生氢气的物质的量是__mol。
②电池Ⅱ属于__电池(填“一次”或“二次”).
③电池Ⅲ是氢氧燃料电池,写出负极的电极反应式是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com