
某常见气体在标准状况下的密度为1.25 g·L![]() 。请填空:
。请填空:
(1)该气体的相对分子质量为 。
(2)若气体的化学式为A2型,其名称为 ;若该气体的化学式为AB型,其名称为 。
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
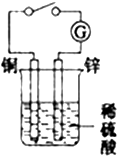 利用铜、锌、稀硫酸、烧杯、导线等设计如下实验:
利用铜、锌、稀硫酸、烧杯、导线等设计如下实验:查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
(1)该气体的相对分子质量为_______。
(2)若气体的化学式为A2型,其名称为________;若该气体的化学式为AB型,其名称为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)该气体的相对分子质量为______。
(2)若气体的化学式为A2型,其名称为______;若该气体的化学式为AB型,其名称为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com