
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7.下列关于滤液中的离子浓度关系不正确的是( )
A.![]() <1.0×10﹣7mol/L
<1.0×10﹣7mol/L
B.c(Na+)=c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3)
)+c(H2CO3)
C.c(H+)+c(NH4+)>c(OH﹣)+c(HCO ![]() )+2 c(CO
)+2 c(CO ![]() )
)
D.c(Cl﹣)>c(HCO ![]() )>c(NH4+)>c(CO
)>c(NH4+)>c(CO ![]() )
)
【答案】D
【解析】解:A.常温下,等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7,说明滤液呈酸性,溶液中c(OH﹣)小于纯水中c(OH﹣), ![]() =c(OH﹣)<1.0×10﹣7mol/L,故A正确; B.任何电解质溶液中都存在物料守恒,碳酸氢铵和NaCl的物质的量相等,虽然析出部分碳B.钠,但仍然存在物料守恒c(Na+)=c(HCO
=c(OH﹣)<1.0×10﹣7mol/L,故A正确; B.任何电解质溶液中都存在物料守恒,碳酸氢铵和NaCl的物质的量相等,虽然析出部分碳B.钠,但仍然存在物料守恒c(Na+)=c(HCO ![]() )+c(CO
)+c(CO ![]() )+c(H2CO3),故B正确;
)+c(H2CO3),故B正确;
C.任何电解质溶液中都存在电荷守恒、物料守恒,根据电荷守恒得c(H+)+c(NH4+)+c(Na+)=c(Cl﹣)+c(OH﹣)+c(HCO ![]() )+2 c(CO
)+2 c(CO ![]() ),根据物料守恒得c(Na+)=c(Cl﹣),则c(H+)+c(NH4+)=c(OH﹣)+c(HCO
),根据物料守恒得c(Na+)=c(Cl﹣),则c(H+)+c(NH4+)=c(OH﹣)+c(HCO ![]() )+2 c(CO
)+2 c(CO ![]() ),因为析出部分钠离子、碳酸氢根离子,所以存在c(H+)+c(NH4+)>c(OH﹣)+c(HCO
),因为析出部分钠离子、碳酸氢根离子,所以存在c(H+)+c(NH4+)>c(OH﹣)+c(HCO ![]() )+2 c(CO
)+2 c(CO ![]() ),故C正确
),故C正确
D.因为析出部分碳酸氢钠,结合物料守恒知滤液中存在c(Cl﹣)>c(HCO3﹣),溶液中析出部分碳酸氢根离子、铵根离子水解但程度较小,所以存在c(HCO ![]() )<c(NH4+),故D错误;
)<c(NH4+),故D错误;
故选D.
A.常温下,等体积、等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7,说明滤液呈酸性,溶液中c(OH﹣)小于纯水中c(OH﹣);
B.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
C.任何电解质溶液中都存在电荷守恒、物料守恒,根据电荷守恒、物料守恒判断;
D.因为析出部分碳酸氢钠,结合物料守恒知滤液中存在c(Cl﹣)>c(HCO ![]() ),溶液中析出部分碳酸氢根离子、铵根离子水解但程度较小.
),溶液中析出部分碳酸氢根离子、铵根离子水解但程度较小.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
【题目】如图为镁-间二硝基苯电池的工作原理示意图。已知:电池放电时,铁转化为氢氧化镁,间二硝基苯则转化为间苯二胺。下列说法不正确的是
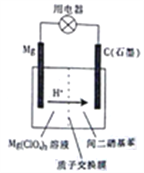
A. 电池放电时,电子由镁电极流出经过用电器流向石墨电极
B. 电池放电时,镁电极附近的电解质溶液的pH降低
C. 电池放电时,理论上每生成1mol间苯二胺就有12molH+通过质子交换膜
D. 电池放电时,石墨电板上发生的反应为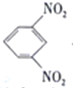 +12H+-12e-=
+12H+-12e-=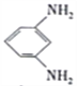 +4H2O
+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化需要加入氧化剂才能实现的是( )
A. HCl → H2 B. NaCl → Cl2 C. CuSO4 → Cu D. HClO → Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下元素周期表,以下说法正确的是
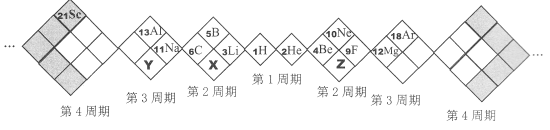
A. X、Y、Z元素分别为N、P、O
B. 所列元素都是主族元素
C. 原子半径:Z>X>Y
D. 稳定性:X的氢化物 < Y的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于同分异构体判断正确的是
A. 分子式为C8H10的芳香烃有3个,分别为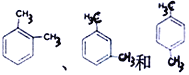
B. C4H10进行一氯取代后生成两种沸点不同的产物
C. C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3
D. 甲苯在一定条件下与氢气加成产物的一氯代物的同分异构体有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的废液经测定其主要含有乙醇,此外还有丙酮、乙酸和乙酸乙酯.以上各物质的沸点如下:
物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
现拟通过下列步骤回收乙醇和乙酸:
①向废液中加入甲溶液;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加入乙溶液(过量),然后再放入蒸馏器中进行蒸馏,收集馏出物.
可选用试剂:A.烧碱溶液 B.浓硫酸 C.饱和食盐水 D.浓盐酸
请回答下列问题:
(1)乙醇的沸点比丙酮沸点高的主要原因是 .
(2)加入甲溶液是 , (填A B C D序号),涉及到的反应方程式: .
(3)在70℃~85℃时馏出物的主要成分为 .
(4)在步骤④中加入过量的乙溶液是 . (填A B C D序号),
(5)最后蒸馏的温度控制在 .
(6)在蒸馏操作中,仪器选择及安装都正确的是:(填标号)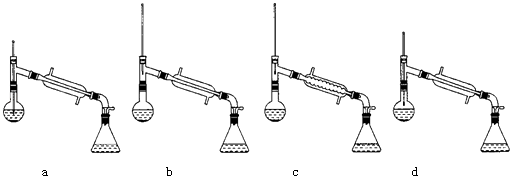
如果蒸馏前忘记加沸石,液体温度已接近沸点时,应该如何处理? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A是短周期中原子半径最小的元素,A、B、C三种元素的原子序数之和等于D元素的原子序数,E是短周期中最活泼的金属元素。下列说法错误的是
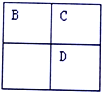
A. 简单离子的半径大小关系:B>C>E
B. 由C、E两种元素组成的两种离子化合物中,阴、阳离子个数比均为1:2
C. C元素的气态氢化物比D元素的气态氢化物稳定是氢键的缘故
D. 已知A、B两种元素组成的离子化合物NH5与水生成气体A2及一种弱碱溶液,推出离子化合物NH5中阴、阳离子个数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,发生反应:2A(g)+B(s)C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( ) ①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内A,C,D三种气体的浓度之比为2:1:1
⑤单位时间内生成n molC,同时生成n mol D
⑥单位时间内生成n molD,同时生成2n mol A.
A.①②⑤
B.②③④
C.②③⑥
D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是元素周期表中前20号元素,原子序数依次增大,A是地壳中含量最高的元素,B、C、D同周期,E和其他元素既不在同一周期也不在同一主族,D的氢化物及其最高价氧化物对应的水化物均为强酸,且B、C、D的最高价氧化物对应的水化物两两混合均能发生反应生成盐和水。据此回答下列问题:
(1)A和D的氢化物中,沸点较低的是 (选“A”或“D”)。
(2)元素C在元素周期表中的位置是 ,B的最高价氧化物对应的水化物的电子式为 。
(3)A、D、E可以形成多种盐,其中一种盐中A、D、E三种元素的原子个数比为2:2:1,该盐的名称为 。它的水溶液与D的氢化物的水溶液反应可生成D的单质,该反应的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com