
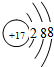 ;
;分析 A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的$\frac{1}{6}$,设最外层电子数为x,则有$\frac{x}{x+2+8}$=$\frac{1}{6}$,解得x=2,故A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al元素,C-离子核外电子层数比A元素的离子核外电子层数多1,则C-离子核外有3层电子,则C为Cl元素;D元素原子最外层电子数是次外层的3倍,则D为O元素;E元素的单质常温下为深红棕色的液体,则E为Br.
解答 解:A、B、C、D四种短周期元素,A元素有三个电子层,其中最外层电子数占总电子数的$\frac{1}{6}$,设最外层电子数为x,则有$\frac{x}{x+2+8}$=$\frac{1}{6}$,解得x=2,故A为Mg元素;B元素原子核外电子数比A元素原子核外电子数多1,则B为Al元素,C-离子核外电子层数比A元素的离子核外电子层数多1,则C-离子核外有3层电子,则C为Cl元素;D元素原子最外层电子数是次外层的3倍,则D为O元素;E元素的单质常温下为深红棕色的液体,则E为Br.
(1)A为Mg元素,E为Br元素,故答案为:Mg;Br;
(2)C原子核内用17个质子,C的负一价阴离子核外各层电子数分别为2、8、8,结构示意图为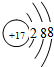 ,故答案为:
,故答案为: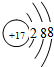 ;
;
(3)氧化铝与氢氧化钠溶液反应生成偏铝酸钠与水,反应离子方程式为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(4)A.将这两种元素的块状单质分别放入冷水中,都不能与冷水反应,故A错误;
B.将这两种元素的单质分别和同浓度的盐酸反应,镁反应较剧烈,可以证明Mg的金属性较强,故B正确;
C.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试液,Mg可以可热水反应,生成Mg(OH)2,溶液呈碱性,而Al难以反应,可证明Mg的金属性较强,故C正确;
D.两种金属元素都不能形成氢化物,故D错误,
故答案为:BC;
(5)同主族自上而下非金属性减弱,故Cl的非金属性>Br元素的非金属性,可以利用单质之间相互置换进行证明,反应方程式为:Cl2+2NaBr=2NaCl+Br2,
故答案为:>;Cl2+2NaBr=2NaCl+Br2.
点评 本题考查位置结构性质的关系及应用,难度不大,注意金属性、非金属性强弱比较实验事实.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题

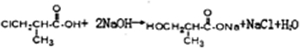 ;高分子化合物H的结构简式为
;高分子化合物H的结构简式为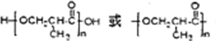 .
.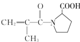 ,F有多种同分异构体,如
,F有多种同分异构体,如 等.写出满足下列条件的F的同分异构体的结构简式:
等.写出满足下列条件的F的同分异构体的结构简式: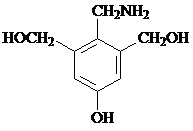 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①②④⑤ | B. | ①②③ | C. | ③④⑤ | D. | ②③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.8 | 2.4 | 0.4 | 放出热量:Q |
| A. | 容器①、②中反应的平衡常数相等,平衡时氮气的转化率相等 | |
| B. | 平衡时,两个容器中NH3 的体积分数均为1/8 | |
| C. | 容器②中达平衡时放出的热量Q=4.63 kJ | |
| D. | 若容器①改为恒压体系,充入0.25 L He,则平衡时放出的热量大于23.15 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入Al能放出H2的溶液中:ClO-、HCO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、NH${\;}_{4}^{+}$ | |
| B. | pH=2的溶液中:Fe2+、Na+、Mg2+、NO${\;}_{3}^{-}$ | |
| C. | 能使KSCN溶液变红的溶液中:Na+、I-、NO${\;}_{3}^{-}$、HCO${\;}_{3}^{-}$ | |
| D. | 由水电离出的c(OH-)=1.0×10-13mol•L-1的溶液中:Na+、Ba2+、Cl-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
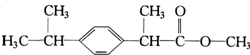 某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )
某种药物主要成分X的分子结构如图,关于有机物X的说法中错误的是( )| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
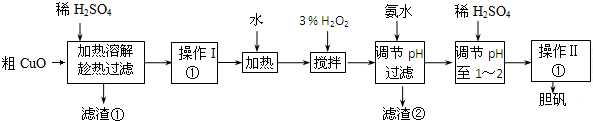
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和NaOH溶液时溶液的pH变大 | |
| B. | 在镀件上电镀铜时,可以不用金属铜做阳极,只要溶液中存在Cu2+就可以 | |
| C. | 电解稀硫酸制O2、H2时,铜做阳极 | |
| D. | 铝-空气燃料电池通常以NaOH溶液为电解液,电池在工作过程中电解液的pH保持不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com