
鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色Fe3+.这个变色的过程中的Fe2+被氧化 (填“氧化”或“还原”).若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生.这说明维生素C具有:B.
A、氧化性 B、还原性 C、酸性 D、碱性.
考点: 氧化还原反应.
专题: 氧化还原反应专题.
分析: 该反应中Fe元素化合价由+2价变为+3价,失电子作还原剂,还原剂发生氧化反应;若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生,说明维生素C能防止亚铁离子被氧化,则维生素C和亚铁离子的性质相同.
解答: 解:该反应中Fe元素化合价由+2价变为+3价,Fe2+失电子作还原剂,在反应中被氧化;若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生,说明维生素C能防止亚铁离子被氧化,则维生素C和亚铁离子的性质相同,都具有还原性,故选B,
故答案为:氧化;B.
点评: 本题考查了氧化还原反应,根据元素化合价升降再结合基本概念分析解答,氧化还原反应的有关概念较多且易混淆,为易错点.


科目:高中化学 来源: 题型:
过氧化氢和臭氧是用途很广的氧化剂。试回答下列问题:
(1) 过氧化氢是一种绿色氧化剂,写出在酸性条件下H2O2氧化氯化亚铁的离子反应方程式:
(2) Na2O2 、K2O2、 以及BaO2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是____________(写电子式),
(3) 臭氧(O3)可以使湿润的淀粉-碘化钾试纸变蓝,反应的化学方程式为:
KI+O3+H2O→KOH+I2+O2(未配平 ) 回答问题:
① 还原产物的化学式为
② 配平后的化学方程式是
(4)O3 可由臭氧发生器(原理如图8所示)电解稀硫酸制得。
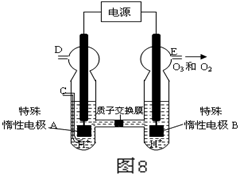

①图中阴极为 (填“A”或“B”)。
② 若C处不通入O 2 ,D、E处分别收集到11.2L和4.48L
气体(标准状况下), 则E处收集的气体中O3所占的体积分数
为 (忽略 O 3 的分解)。
③ 若C处通入O 2,则A极的电极反应式为: 。
(5)新型O3氧化技术对燃煤烟气中的NOx和SO2脱除效果显著,锅炉烟气中的NOx 95%以上是以NO形式存在的,可发生反应NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如图9)所示。由图可得出的正确说法是
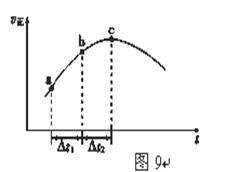
a.反应在c点达到平衡状态
b.反应物浓度:b点小于c点
c.反应物的总能量低于生成物的总能量
d.Δt1=Δt2时,NO的转化率:a~b段小于b~c段
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式的是()
A. 氢氧化钡溶液与盐酸的反应 2OH﹣+2H+=2H2O
B. 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O
C. 铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag
D. 碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
有甲、乙、丙三种试液,在氢氧化钡溶液中加入甲有白色沉淀生成,在沉淀中加入乙,沉淀完全溶解并产生气泡,最后向所得溶液中加入丙又产生白色沉淀,则甲、乙、丙依次是()
A. K2CO3、HCl、CaCl2 B. Na2CO3、HNO3、MgSO4
C. Na2CO3、HCl、Ba(NO3)2 D. H2SO4、Na2CO3、AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 英国科学家道尔顿发现了元素周期律
B. 研究物质性质的基本方法有实验法、观察法、分类法、比较法
C. 化学的特征是认识分子和制造分子
D. 我国科学家合成的结晶牛胰岛素是世界上首次人工合成的具有生物活性的蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中不属于氧化还原反应是()
A. H2+CuO  Cu+H2O
Cu+H2O
B. Ca2++CO32﹣═CaCO3↓
C. 3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O
D. 2H2O2 2H2O+O2↑
2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的HCl气体6.72L溶于水配成500ml盐酸溶液,
(1)该盐酸溶液的物质的量浓度
(2)取该盐酸400ml和足量的碳酸钙完全反应后生成的CO2气体在标况下的体积为多少?(写计算过程)
(3)将生成的CO2气体通入到一定量的Na2O2固体中,充分反应后固体质量比原增加1.4g,则参加反应的CO2气体的物质的量为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学按下列步骤配制500mL 0.20mol•L﹣1KCl溶液,请回答有关问题.
实验步骤 有关问题
(1)计算所需KCl的质量
需要KCl的质量为
(2)称量 固体 称量过程中主要用到的仪器是
(3)将KCl加入100mL烧杯中,加适量蒸馏水溶解 为加快溶解,可采取的措施是
(4)将烧杯中的溶液转移至500mL容量瓶中 为防止溶液溅出,应该采取的措施是
(5)向容量瓶中加蒸馏水至刻度线 在进行此操作时应注意的问题是
你认为按上述步骤配制的KCl溶液的浓度是否为0.200mol•L﹣1,请说明理由. .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com