
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示:
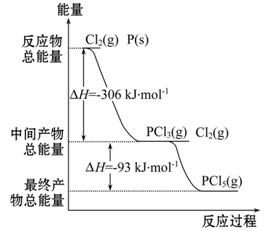
(图中的ΔH表示生成1 mol产物的数据)。
(1)P和Cl2反应生成PCl3的热化学方程式是____________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式是__________ _______________。
_______________。
(3)P和Cl2分两步反应生成1 mol PCl5的ΔH3=__________,P和Cl2一步反应生成1 mol PCl5的ΔH4_ ______________ΔH3 (填“大于”“小于”或“等于”)。
______________ΔH3 (填“大于”“小于”或“等于”)。
(4)PCl5与足量水充分反应,最终生成两种酸,其化学方程式是______________。
(1)(2)反应物和反应产物互换时,ΔH数值不变,注意变号。
(3)总反应的焓变,可以看做是各步反应焓变的加和。
(4)PCl5与水反应时,化合价未发生变化,可依此分析出酸为磷酸和盐酸。
科目:高中化学 来源: 题型:
下列说法中,正确的是
A.胆矾、漂白粉、氯化钾、石墨四种物质分别是按纯净物、混合物、电解质和非电解质的类别顺序排列的。
B.强电解质均是离子化合物
C.碱性氧化物一定是金属氧化物
D.酸性氧化物一定是非金属氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
书写离子方程式(8分)
(1) 铜和足量浓硝酸反应的离子方程式为
(2)二氧化锰与足量浓盐酸反应的离子方程式为:
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:
(4)向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,抽去右图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是(设NA表示阿伏加德罗常数的值)
A.气体反应物的总体积为0.448L
B.装置中氢元素的总质量为0.04g
C.生成物中含有0.01NA个分子
D.生成物完全溶于水后所得溶液含有0.01 NA个NH4 +
查看答案和解析>>
科目:高中化学 来源: 题型:
用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:
(1)计算机芯片的主要成分是________。
(2)光导纤维的主要成分是________。
(3)目前应用最多的太阳能电池的光电转化材料是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是
A.密度比为16∶11 B.分子个数比为16∶11
C.体积比为1∶1 D.氧原子个数比为1∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com