
| A. | 浓硫酸稀释时,应该将浓硫酸沿着烧杯内壁慢慢注入装有水的烧杯中,并不断搅拌 | |
| B. | 不慎将汞滴落到桌面上,应立即用抹布抹掉,再用较多的水冲洗 | |
| C. | 甲烷易燃烧,点燃前要验纯,乙烯可以直接点燃 | |
| D. | 镁着火时可用二氧化碳扑灭 |
分析 A.浓硫酸稀释过程中放出大量热,且浓硫酸密度大于水,据此判断正确的稀释方法;
B.应撒上硫粉覆盖;
C.不纯甲烷点燃时容易发生爆炸;
D.二氧化碳能够支持镁燃烧.
解答 解:A.浓硫酸密度大于水,稀释会放出大量热,所以稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌,故A正确;
B.应撒上硫粉覆盖,硫与汞反应生成难挥发的硫化汞,故B错误;
C.若是不验纯,容易发生爆炸的危险,故C错误;
D.二氧化碳能够支持镁燃烧,镁着火不能用二氧化碳扑灭,故D错误.
故选A.
点评 本题考查了化学实验安全事故及处理方法、浓硫酸的性质,题目难度不大,注意掌握化学实验基本操作方法,明确浓硫酸的酸性、强氧化性的判断方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4mol N2 |
| 达到平衡的时间(min) | t | 5 |
| 平衡时N2的浓度(mol•L-1) | 3 | c |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  实验室中制取少量的乙酸乙酯 | |
| B. |  比较硫、碳、硅三种元素的非金属性强弱 | |
| C. |  处理尾气 | |
| D. | 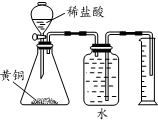 测定黄铜(Cu、Zn合金)中Zn 的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铝片加入浓硫酸中,探究Al的活泼性 | |
| B. | 将NaOH溶液缓慢滴入Al2(SO4)3溶液中,观察Al (OH)3沉淀的生成及溶解 | |
| C. | 将Al(OH)3浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 | |
| D. | 将Al(OH)3沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水AlCl3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Cu投入稀硫酸中 | |
| B. | 让Cu在潮湿的环境发生电化学腐蚀 | |
| C. | 将Cu投入浓硫酸中并加热 | |
| D. | 用Cu作电极、稀硫酸作电解质溶液电解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com