
【题目】某矿物甲由常见的三种元素组成,有如下变化。请回答下列问题:

(1)甲的化学式为_________。
(2)写出矿物甲与过量稀H2SO4/O2反应的离子方程式__________________。
(3)用文字叙述检验纯净的盐中的阳离子(写出实验操作、现象及结论)_________________。
【答案】 FeCuS2 4FeCuS2+l7O2+4H+=4Fe3++4Cu2++8SO42-+2H2O 取少量纯净的盐溶于水,滴加KSCN溶液,溶液不变色,冉滴加H2O2溶液(或氯水),溶液变成血红色,说明盐中的阳离子是Fe2+
【解析】试题分析:矿物甲与过量的硫酸、氧气反应后的溶液加入铁粉,生成的气体单质是氢气;生成的红色固体是铜;得到的溶液中含有一种盐,一定是硫酸亚铁;根据元素守恒,矿物甲含有铁元素、铜元素、硫元素;
解析:生成氢气的反应为![]() ,根据生成0.1mol氢气,参加反应的铁的物质的量为0.1mol;生成铜的方程式为
,根据生成0.1mol氢气,参加反应的铁的物质的量为0.1mol;生成铜的方程式为![]() ,根据铜的质量可知,原固体矿物中含有0.2mol的铜元素,参加反应的铁的物质的量为0.2mol;根据铁元素守恒,
,根据铜的质量可知,原固体矿物中含有0.2mol的铜元素,参加反应的铁的物质的量为0.2mol;根据铁元素守恒, ![]() 反应生成Fe2+ 0.6-0.3=0.3mol,原矿物中铁元素的物质的量为0.2mol;原矿物中硫元素的质量为36.8-0.2mol×64g/mol-0.2mol×56g/mol=12.8g,硫元素的物质的量是0.4mol。(1)铁:铜:硫=0.2:0.2:0.4=1:1:2;所以甲的化学式为FeCuS2;(2)FeCuS2与过量稀H2SO4/O2反应的离子方程式是4FeCuS2+l7O2+4H+=4Fe3++4Cu2++8SO42-+2H2O;(3)纯净的盐中含有阳离子是Fe2+,检验Fe2+的方法是取少量纯净的盐溶于水,滴加KSCN溶液,溶液不变色,冉滴加H2O2溶液(或氯水),溶液变成血红色,说明盐中的阳离子是Fe2+。
反应生成Fe2+ 0.6-0.3=0.3mol,原矿物中铁元素的物质的量为0.2mol;原矿物中硫元素的质量为36.8-0.2mol×64g/mol-0.2mol×56g/mol=12.8g,硫元素的物质的量是0.4mol。(1)铁:铜:硫=0.2:0.2:0.4=1:1:2;所以甲的化学式为FeCuS2;(2)FeCuS2与过量稀H2SO4/O2反应的离子方程式是4FeCuS2+l7O2+4H+=4Fe3++4Cu2++8SO42-+2H2O;(3)纯净的盐中含有阳离子是Fe2+,检验Fe2+的方法是取少量纯净的盐溶于水,滴加KSCN溶液,溶液不变色,冉滴加H2O2溶液(或氯水),溶液变成血红色,说明盐中的阳离子是Fe2+。


科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在水溶液中大量共存的是( )
A.I-、K+、ClO-、OH-B.Fe2+、H+、SO42-、NO3-
C.Al3+、K+、HCO3-、OH-D.Na+、Mg2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)(1)浓H2SO4能够用于干燥某些气体,是由于它具有 性;下列气体能用浓硫酸来进行干燥的气体是 (可多选,但只要有选错项,即得0分)① Cl2 ② H2S ③ NH3 ④ CO2
(2)浓H2SO4能使纸片变黑,是由于它具有 性;
(3)浓H2SO4可以与Cu反应,是由于它具有 性和 性,其反应的化学方程式是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是一座开放的“元素大厦”,元素大厦尚未客满。请你在元素大厦中为119号元素安排好它的房间
A. 第八周期第IA族 B. 第七周期第ⅦA族
C. 第七周期第0族 D. 第六周期第ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某纯天然食用香料X是一种从植物中提取的芳香族化合物,由香料X合成有机物H的路线如图所示:
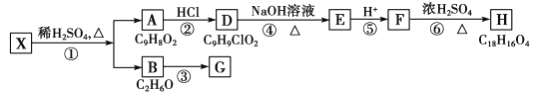
已知:①A的核磁共振氢谱显示有6组峰;②H为酯类物质,结构中除苯环外还含有一个六元环; ③G的产量是衡量一个国家石油化工发展水平的标志。
请回答下列问題:
(1)A的结构简式为______,检验A中非含氧官能团所用的试剂为______。
(2)②的反应类型为______。反应③的化学方程式为______
(3)F中所含官能团的名称为______,其同分异构体中,遇FeCl3溶液发生显色反应,且能与碳酸氢钠溶液反应,其苯环上一氯代物只有一种,符合条件的同分异构体数目为______种,写出其中一种的结构简式:______。
(4)设计一条以G为起始原料合成乙二醛的路线,无机物任选,注明反应条件。示例如下:
![]() ___________
___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com