
【题目】有机物A分子中含苯环,相对分子质量136,分子中碳、氢原子个数相等,其含碳质量分数为70.6%,其余为氧、氢。
(1)A的分子式是__________________。
(2)若A分子中能发生银镜反应,且有弱酸性,则A的同分异构体有_______种,请任写一种符合条件的A的结构简式: 。
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的说法正确的是( )。
A. 可用25mL碱式滴定管量取20.00mL KMnO4溶液
B. 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C. 将金属钠在研钵中研成粉末,使钠与水反应的实验更安全
D. 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的![]() ,液体也不能蒸干
,液体也不能蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只可能含有下列离子中的几种(不考虑溶液中含有的较少的H+和OH-):Na+、NH4+、SO42-、CO32-、NO3-。取200 mL该溶液,分为两等份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加足量的BaCl2溶液,得固体2.33g。下列说法正确的是
A.该溶液中可能含有Na+
B.该溶液中肯定含有NH4+、SO42-、CO32-、NO3-
C.该溶液中一定不含NO3-
D.该溶液中一定含Na+,且c(Na+) ≥ 0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容器可变的密闭容器中,反应N2(g)+3H2(g)![]() 2NH3(g)在一定条件下达到平衡。完成下列填空:
2NH3(g)在一定条件下达到平衡。完成下列填空:
(1)在其他条件不变的情况下,缩小容器体积以增大反应体系的压强,v正______(选填“增大”、“减小”,下同),v逆______,平衡向______方向移动(选填“正反应”、“逆反应”)。
(2)在其他条件不变的情况下,降低温度平衡向正反应方向移动,为______反应(选填“吸热”、“放热”)。
(3)如图为反应速率(ν)与时间(t)关系的示意图,由图判断,在t1时刻曲线发生变化的原因是______(填写编号)。

a.增大N2的浓度 b.扩大容器体积 c.加入催化剂 d.升高温度
改变条件后,平衡混合物中NH3的百分含量______(选填“增大”、“减小”、“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:一定条件下,向一个密闭容器中加入0.30molX、0.10molY和一定量的Z三种气体,甲图表示发生反应后各物质浓度(c)随时间(t)的变化〔其中t0~t1阶段c(Z)未画出〕。乙图表示化学反应速率(v)随时间(t)的变化,四个阶段都只改变一种条件(催化剂、温度、浓度、压强,每次改变条件均不同),已知t3~t4阶段为使用催化剂。
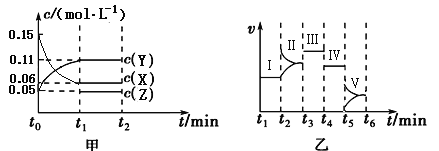
回答下列问题:
(1)若t1=5 min,则t0~t1阶段以X浓度变化表示的反应速率为v(X)= 。
(2)在t2~t3阶段Y的物质的量减小,则此阶段开始时v正 v逆(填“>”、“=”或“<”)。
(3)t4~t5阶段改变的条件为 ,此阶段的平衡常数K = 。
(4)t5~t6阶段容器内Z的物质的量共增加0.10 mol,在反应中热量变化总量为a kJ,写出该反应的热化学方程式 。在乙图Ⅰ~Ⅴ处平衡中,平衡常数最大的是 。
(5)若起始实验条件不变,重新向该容器中加入0.60 mol X、0.20 mol Y和0.080 mol Z,反应至平衡状态后X的转化率= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为甲同学设计的制取并检验C2H4性质的实验装置图。请回答有关问题:
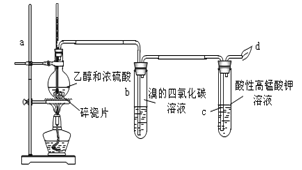
(1)写出上述制乙烯的反应的化学方程式: ,
(2)加入几片碎瓷片的目的是 ,
(3)加热时,使混合液温度迅速升高到170℃,是为了 ,
(4)实验过程观察到的现象为:
①Br2的四氯化碳溶液由 色变 ,
②酸性KMnO4溶液 。
(5)乙同学认为甲同学设计的实验如果仅从酸性KMnO4溶液褪色难以证明反应有乙烯生成,因为反应产生的乙烯中可能混有 气体也能使酸性KMnO4溶液褪色。写出此气体使酸性KMnO4溶液褪色的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸按是一种常用的化肥,其工业生产流程如下图,请回答下列问题。

(1)写出反应容器B中发生反应的化学方程式: 。
(2)吸收塔C中通入空气的目的是 。C、D两个反应容器中发生的反应,属于氧化还原反应的是 (填反应容器代号)。
(3)浓硝酸一般保存在徐色试剂瓶里,并放置在阴凉处,用化学方程式解释原因: 。
(4)3.04g铜镁合金完全溶解于100mL密度为1.40g·mL-1、质量分数为63%的浓硝酸中得到NO2和N2O4的混合气体2240mL(标准状况),向反应后的溶液中加入2.00mol·L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀。则
① 加小Na0H 溶液的体积至少 mL。
② 该合金中铜与镁的物质的量之比是 。
③ NO2和N2O4的混合气体中,NO2的体积分数是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率减小;当减小压强时,混合体系中A的质量分数增大,则
pC(g),达到平衡后,当升高温度时,B的转化率减小;当减小压强时,混合体系中A的质量分数增大,则
(1)该反应的正反应是__________热反应,且m+n__________p (填“>”、“<”或“=”)。
(2)增大压强时,B的转化率__________(填“增大”、“减小”或“不变”,下同),逆反应速率__________。
(3)若加入C(体积不变),则A的体积分数__________。
(4)若降低温度,则平衡时B、C的浓度之比c(C)/c(B)比值将________。
(5)若加入催化剂,该反应的反应热________。
(6)若B是有色物质,A、C均为无色物质,维持容器体积不变,充入氖气时,混合气体的颜色__________(填“变浅”、“变深”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡用作媒染剂和有机合成上的氯化催化剂,甲、乙为实验室制备四氯化锡的反应装置示意图,有关信息数据如下:

有关信息数据:①实验室制备四氯化锡的操作是将金属锡熔融,然后泼入冷水,制成锡花,将干燥的锡花加入反应器中,再向反应器中缓缓通入干燥氯气;②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃,③无水四氯化锡暴露于空气中与空气中的水分反应生成白色烟雾,有强烈的刺激性。请回答下列问题:
Ⅰ、图甲是实验室制备干燥氯气的实验装置(夹持装置已略)
(1)A的仪器名称为__________,该装置制备氯气选用的药品为漂粉精固体[主要成分Ca(ClO)2]和浓盐酸,B中发生反应的化学方程式为__________。
(2)装置C中饱和食盐水的作用是__________,同时装置C亦是安全瓶,能检测实验进行时是否发生堵塞,请写出发生堵塞时C中的现象:__________。
(3)试剂X可能为__________(填序号)
A无水氯化钙 B浓硫酸 C.碱石灰 D五氧化二磷
(4)用锡花代替锡粒的目的是__________。
Ⅱ.图乙是蒸馏SnCl4的装置
(1)图中,收集到的SnCl4中可能存在的副产物的化学式为__________。
(2)该装置尚有两处不当之处,它们分别是__________,__________;
(3)若实验中用去锡粉5,95g,反应后,Ⅱ中锥形瓶里收集到12.0gSnCl4。则SnCl4的产率为__________。(结果保留3位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com