
| |||||||||||||||||||||||||||
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:许昌市2006-2007学年度上学期四校第二次联考 高一化学试题 题型:013
|
工业上常用金属钠来提炼钛、锆等.已知在700℃-800℃时,钠可从四氯化钛(TiCl4)中还原出钛,则用此法制取96 g钛时需要钠的理论质量为 | |
| [ ] | |
A. |
11.5 g |
B. |
23 g |
C. |
184 g |
D. |
92 g |
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高一版(必修1) 2009-2010学年 第10期 总第166期 人教课标版 题型:022
(1)用金属钠制取Na2O通常采用以下方法:2NaNO3+10Na![]() 6Na2O+N2↑.试说明不用钠在氧气中燃烧而采用此法的原因:________.
6Na2O+N2↑.试说明不用钠在氧气中燃烧而采用此法的原因:________.
(2)金属钠在700℃~800℃时与四氯化钛(TiCl4)反应可以制取金属钛,该反应的化学方程式为________.
查看答案和解析>>
科目:高中化学 来源:江苏省前黄高级中学2007届高三年级第一学期期中考试、化学试卷 题型:022
| |||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
图1-5-17是实验室制备TiCl4的反应装置,主要操作步骤为:
①连接好整套装置,在通Cl2前先通入CO2气体并持续一段时间;
②当锥形瓶中TiCl4的量不再增加时,停止加热,从侧管中改通CO2气体直到电炉中的瓷管冷却为止;
③将TiO2、炭粉混合均匀后,装入管式电炉中;
④将电炉升温到800℃,一段时间后改通Cl2,同时在冷凝管中通冷凝水。
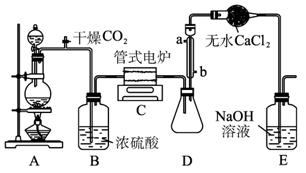
图1-5-17
试完成下列各题:
(1)正确的操作顺序为(填序号)_______________________________________________。
(2)装置A中的反应的离子方程式为__________________________________________。
(3)操作①的目的是_________________________________________________________。
(4)装置D中冷凝管进水口的位置是________(填a或b),装置E的作用是________________
____________________________________________________________________。
(5)TiCl4露置于空气中极易水解,其化学方程式可表示为_________________________。
(6)工业上常用金属镁在800℃和氩气氛围中还原TiCl4的方法制备钛,TiCl4+2Mg![]()
Ti+2MgCl2,氩气的作用为___________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届江西省抚州市高二下学期期末考试化学试卷(解析版) 题型:填空题
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成为是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色) +Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是 。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在 范围。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可以制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K=
。
Fe3++3H2O的平衡常数K=
。
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: 。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是 (只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4的,可采用 方法。
|
|
TiCl4 |
SiCl4 |
|
熔点/℃ |
-25.0 |
-68.8 |
|
沸点/℃ |
136.4 |
57.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com