
| A. | FeCl3 | B. | 浓硫酸 | C. | NaCl | D. | NaNO3 |
分析 铜的化学性质不活泼,不能与非氧化性酸反应,但可以和氧化性酸反应,能与具有氧化性的FeCl3溶液、酸性条件下硝酸盐等反应,据此判断选项.
解答 解:A.三价铁离子具有强的氧化性,能够与铜反应生成可溶性铜离子和二价铁离子,铜片溶解,没有气泡产生,故A不选;
B.铜与浓硫酸只有在加热条件下才能发生反应,所以常温下向稀硫酸中加入铜片,无现象,向溶液中继续加入浓硫酸,铜与浓硫酸也不会发生反应,铜片不溶解,不会产生气体,故B不选;
C.向稀硫酸溶液中加入氯化钠后,溶液中不存在与铜反应的物质,铜片不溶解,不会产生气体,故C不选;
D.硝酸根离子在酸性环境下具有强的氧化性,加入硝酸钠后,发生反应的离子方程式:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,铜片溶解同时生成一氧化氮气体,故D选;
故选:D.
点评 本题考查了物质之间的反应,熟悉铜、硝酸的性质是解题关键,注意铜与浓硫酸发生反应需要加热,题目难度不大.


科目:高中化学 来源: 题型:选择题
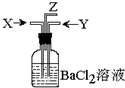 碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )
碳跟浓硫酸共热产生的气体X和二氧化锰跟浓盐酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是…( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | |
| B. | 在Z导管出来的气体中无二氧化碳 | |
| C. | 洗气瓶中产生的沉淀是硫酸钡 | |
| D. | 洗气瓶中产生的沉淀是碳酸钡和亚硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强氧化性和脱水性 | B. | 强氧化性和吸水性 | ||
| C. | 难挥发性和酸性 | D. | 脱水性和吸水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、K+、Ba2+、Cl- | B. | Na+、K+、Cl-、SiO32- | ||
| C. | SO42-、Na+、Cu2+、Cl- | D. | SO42-、NO3-、K+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
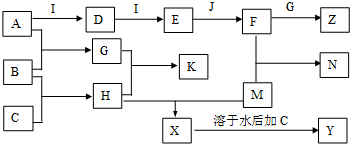
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
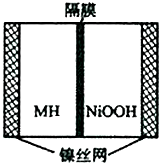 如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )
如图是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MH-Ni电池).该电池放电时的总反应为:MH+NiOOH=M+Ni(OH)2,下列有关说法不正确的是( )| A. | 放电时负极反应为:MH+OH--e-→M+H2O | |
| B. | 电池的电解液可为KOH溶液,OH-向负极移动 | |
| C. | 放电时正极反应为:NiOOH+H2O-e-→Ni(OH)2+OH- | |
| D. | MH是一类储氢材料,其氢密度越大,电池的能量密度越高 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
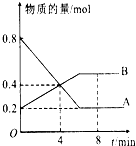 某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据
某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C10H1202的有机物,①苯环上有两个取代基,②能与NaHCO3反应生成气体,满足以上2个条件的该有机物的同分异构体有15种 | |
| B. | 分子式为C4H8Cl2机物,只含有一个甲基的同分异构体有7种 | |
| C. | 分子式为C4H10O的醇,能在铜催化下被O2氧化为醛的同分异构体有4种 | |
| D. |  分子中的所有原子有可能共平面 分子中的所有原子有可能共平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com